Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 23. 11. 2011 15:59
- janca361

- .
- Příspěvky: 3284
Změna vnitřní energie plynu
Ahoj, mám příklad:
Jak se změní vnitřní energie helia o hmotnosti 10 g, jestliže se jeho teplota zvýší o 100°C? Relativní atomová hmotnost helia He je 4, atomová hmotnostní konstanta je  a Boltzmanova konstanta je
a Boltzmanova konstanta je  . [3,1 kJ]
. [3,1 kJ]
Jak se počítá  ? O:-)
? O:-)
Děkuji.
Offline
- (téma jako vyřešené označil(a) janca361)
#2 23. 11. 2011 16:10
Re: Změna vnitřní energie plynu
↑ janca361:
Vše prozradil Zdeněk zde. Střední kinetická energie 1 částice je  .
.
Offline
#3 23. 11. 2011 16:28
- janca361

- .
- Příspěvky: 3284
Re: Změna vnitřní energie plynu
↑ LukasM:
Teď už nějak chápu to, co Zdeněk napsal. Na začátku října to bylo: "CO?" a přislo mi to, že zachází do příšerných detailů :) Teď už některé vztahy znám, teda spíš už jsem viděla a měla bych znát (ale tím, že je znám si nejsem občas moc jistá...)
Zatím díky.
Offline
#4 23. 11. 2011 16:49
- janca361

- .
- Příspěvky: 3284
Re: Změna vnitřní energie plynu
zdenek1 napsal(a):
↑↑ janca361:
u ideálního plynu se vzájemná potenciální energie částic zanedbává ->
kinetická je součet kinetických energií jednotlivých částic ->(tohle platí pro všechna skupenství, ale prakticky je to k ničemu)
Dále se definuje střední kvadratická rychlost tak, že(pokud jsou všechny částice identické co do hmotnosti)
podle ekvipartičního teorému pak je, takže
(Protože
)
 - jak se tam objevilo
- jak se tam objevilo  ?
?
Offline
#5 23. 11. 2011 16:53
Re: Změna vnitřní energie plynu
↑ janca361: N je počet částic - tohle platí pro 1 částici, tak to musíš ještě vynásobit jejich počtem
- tohle platí pro 1 částici, tak to musíš ještě vynásobit jejich počtem
Radim, tedy jsem.
Dobrá rada je drahá, ta moje je zdarma.
Offline
#6 23. 11. 2011 16:53
Re: Změna vnitřní energie plynu
↑ janca361:
No, to by mělo být jasné. Pokud m je hmotnost jedné částice a  její střední kvadratická rychlost, pak střední kinetická energie jedné částice je
její střední kvadratická rychlost, pak střední kinetická energie jedné částice je  . No, a protože částic máme N...
. No, a protože částic máme N...
Ale jdeš na to ze špatné strany, protože neznáš  . Použij přímo ten vzorec co jsem ti poslal. Samozřejmě tam můžeš za
. Použij přímo ten vzorec co jsem ti poslal. Samozřejmě tam můžeš za  dosadit, pokud ji z mého vzorce vyjádříš, ale je to cesta strašně okolo.
dosadit, pokud ji z mého vzorce vyjádříš, ale je to cesta strašně okolo.
Offline
#7 23. 11. 2011 17:13
#8 23. 11. 2011 17:21
Re: Změna vnitřní energie plynu
↑ janca361:
Ten skrytý text je špatně. Přehodila jsi ten zlomek.
V zásadě do toho není potřeba tahat pojem látkové množství. Máme 10g něčeho, známe relativní at. hmotnost - to znamená, že víme, že jeden atom váží 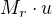 . Takže dopočítat počet atomů je přímočaré.
. Takže dopočítat počet atomů je přímočaré.
A i zde si dávej pozor na záměnu molární hmotnosti a relativní atomové hmotnost.
Offline
#9 23. 11. 2011 17:31
- janca361

- .
- Příspěvky: 3284
Re: Změna vnitřní energie plynu
LukasM napsal(a):
A i zde si dávej pozor na záměnu molární hmotnosti a relativní atomové hmotnost.
No jó. 

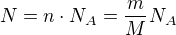
LukasM napsal(a):
Máme 10g něčeho, známe relativní at. hmotnost - to znamená, že víme, že jeden atom váží
. Takže dopočítat počet atomů je přímočaré. Takže dopočítat počet atomů je přímočaré.
Ale já nějak nevím, jak to počítat :(
Určitě se to dá jinak než jsme to počítala já, jinak by v zadání nebylo 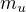 .
.
Objevila jsem ještě vztah: 
To by se taky mohlo dát použít.
Offline
#10 23. 11. 2011 17:41 — Editoval LukasM (23. 11. 2011 17:42)
Re: Změna vnitřní energie plynu
↑ janca361:
Jak to počítat dle mého návrhu? Máme 1000 litrů mlíka a jeden půllitr. Kolikrát můžu vypít jeden půllitr, než mi dojde mlíko? (je to jen hypotetická otázka, praktickou realizaci by pravděpodobně znemožnily střevní obtíže)
No, a pak si znova přečti tu mou větu co jsi citovala, a měla bys vidět, jak spočítáš atomy.
Edit:  tohle mi není úplně jasné.
tohle mi není úplně jasné.
Offline
#11 23. 11. 2011 17:48
- janca361

- .
- Příspěvky: 3284
Re: Změna vnitřní energie plynu
1000 litrů mlíka.....žeby  ?
?
půl litr...... nebo
nebo 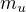 (
( )
)
? -mě to taky není jasné :) Tak to tedy tak řešit nebudu
-mě to taky není jasné :) Tak to tedy tak řešit nebudu
Offline
#12 23. 11. 2011 17:58
Re: Změna vnitřní energie plynu
↑ janca361:
:-) Nechceš mi tvrdit, že na tu mou otázku nedokážeš odpovědět, že ne? Kolikrát se můžu napít? Nehledej analogie mezi mlíkem a těmi ostatními veličinami, ale prostě odpověz kolikrát. A až to uděláš, tak mi řekni, jak jsi to spočítala.
Až to budeš mít, tak si teprve znovu přečti větu "máme 10g něčeho, a to něco je složené z dílečků, které váží každý  ." A pak snad uvidíš, jak spočítat počet dílečků.
." A pak snad uvidíš, jak spočítat počet dílečků.
Offline
#14 23. 11. 2011 18:29
Re: Změna vnitřní energie plynu
↑ janca361:
Ano, k tomu jsem mířil. Akorát je potřeba dodržet jednotky, tedy buď dosadit 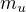 v gramech, nebo místo 10 v čitateli psát 0,01.
v gramech, nebo místo 10 v čitateli psát 0,01.
Offline
#16 23. 11. 2011 18:36 — Editoval LukasM (23. 11. 2011 18:39)
Re: Změna vnitřní energie plynu
↑ janca361:
Ano. Jinak mlíko, krychličky a podobné nesmysly na tebe vytahuju ne proto, že bych z tebe chtěl dělat tele, ale protože mám pocit, že u všeho moc slepě hledáš nějaké vzorečky, do kterých chceš dosadit a nazdar. Někdy je lepší se jen trochu zamyslet a zjistíš, že polovina všech těch vzorečků jsou zbytečnosti, na které vždycky přijdeš sama.
Edit: jo, zajímavá věc. Když si porovnáš ty dva postupy, tak zjistíš, že  . Není to vzrušující? Je to právě těch
. Není to vzrušující? Je to právě těch 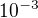 , o které se liší molární hmotnost a relativní atomová hmotnost. Takže to vzrušující je.
, o které se liší molární hmotnost a relativní atomová hmotnost. Takže to vzrušující je.
Offline
#17 23. 11. 2011 18:49
- janca361

- .
- Příspěvky: 3284
Re: Změna vnitřní energie plynu
LukasM napsal(a):
↑ janca361:
Edit: jo, zajímavá věc. Když si porovnáš ty dva postupy, tak zjistíš, že. Není to vzrušující? Je to právě těch
, o které se liší molární hmotnost a relativní atomová hmotnost. Takže to vzrušující je.
Ne, není. A jaktože se  liší od
liší od  , když se mají číselně rovnat?
, když se mají číselně rovnat?
Vpohodě, mě je jasný, že ze mě nechceš dělat blbce ;) Přiznám se, že někdy tam ty vzorečky opravdu hledám ;)
Offline
#18 23. 11. 2011 19:04
Re: Změna vnitřní energie plynu
↑ janca361:
Liší se? Jakto? Relativní at. hmotnost se má číselně rovnat molární hmotnosti v gramech.
Jeden vzorec pro výpočet byl  , druhý byl
, druhý byl  . Schválně je zkus dát do rovnosti, a vyjádřit
. Schválně je zkus dát do rovnosti, a vyjádřit  .
.
Nebo jak jsi přišla na to, že to nesedí?
Offline
#20 23. 11. 2011 19:14
Re: Změna vnitřní energie plynu
↑ janca361:
Jo, už chápu. Tys reagovala jen na tu mou větu, já jsem nějak myslel že jsme ještě u toho příkladu.
No, liší se. Nemůžeš jen tak napsat číselnou hodnotu relativní at. hmotnosti místo molární hmotnosti, protože molární hmotnost ten vzorec "čeká" v kg.
Offline
#22 23. 11. 2011 19:51
Re: Změna vnitřní energie plynu
↑ janca361:
Ne ne, počítají ve stejných. Ale  nemá význam hmotnosti, nemá jednotku, nemůžeš to jen tak použít jako hmotnost. Pokud se to rozhodneš udělat, tak to sice nějak vyjde, ale musíš dát pozor na to, jak přesně to uděláš.
nemá význam hmotnosti, nemá jednotku, nemůžeš to jen tak použít jako hmotnost. Pokud se to rozhodneš udělat, tak to sice nějak vyjde, ale musíš dát pozor na to, jak přesně to uděláš.
Takže mám nějaký vzorec, ve kterém figuruje molární hmotnost (kterou bych dosadil dejme tomu v kg), ale chci to nějak přečůrat a použít  . Je to možné, ale dosazuju bezrozměrné číslo někam, kam jsem měl dosadil něco, co má jednotku. Tím pádem se musím o jednotku postarat sám. Vím, že
. Je to možné, ale dosazuju bezrozměrné číslo někam, kam jsem měl dosadil něco, co má jednotku. Tím pádem se musím o jednotku postarat sám. Vím, že  je číselně rovna
je číselně rovna  vyjádřené v g (
vyjádřené v g (![kopírovat do textarea $M_m [g]=M_r$](/mathtex/d5/d5386d0ff9f63a4624a41a56ac9385aa.gif) ). Takže číselná hodnota molární hmotnosti v kilogramech je
). Takže číselná hodnota molární hmotnosti v kilogramech je  (tisíckrát menší) - a to je to co použiju do toho svého vzorce.
(tisíckrát menší) - a to je to co použiju do toho svého vzorce.
Takže počítám dejme tomu látkové množství:  . Teď mám dvě možnosti. Buď se budu držet základních jednotek,, m dosadím v kg, a místo
. Teď mám dvě možnosti. Buď se budu držet základních jednotek,, m dosadím v kg, a místo  napíšu
napíšu  , nebo dosadím m v gramech, a místo
, nebo dosadím m v gramech, a místo  napíšu přímo
napíšu přímo  .
.
Celé je to po formální stránce trochu prasárna, protože počítáš jen s číselnými hodnotami, a ty jednotky máš jen v hlavě.
Offline



 =>
=> 






 ?
?![kopírovat do textarea $[M]=g \cdot mol ^{-1}$](/mathtex/68/6813b64eb8b372e5b68d3454bfa1b673.gif)