Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 21. 12. 2011 18:26
spalné teplo anthracenu
Zdravím,
mám problém s vypočítáním tohoto příkladu:
2,326 g vzorku anthracenu je vložen do kalorimetru a spálen. Tepelná kapacita kalorimetru je 1,626 kJ/°C a obsahuje 1,148 kg vody. Jaké je spalné teplo anthracenu, když se teplota vody zvýší z 24,126°C na 38,667°C? (Molární kapacita vody: 75,29 J/(°C*mol))
Vypočítala jsem 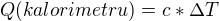
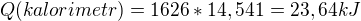
poté jsem vypočítala 
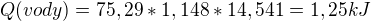
pak jsem spočítala 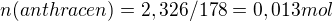
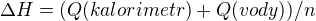
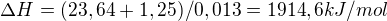
Ve výsledku je uvedeno zhruba 7000 kJ/mol. Mám chybu v postupu řešení? Děkuji
Offline
- (téma jako vyřešené označil(a) Sydnney)
#2 21. 12. 2011 18:42 — Editoval smatel (21. 12. 2011 18:43)
Re: spalné teplo anthracenu
↑ Sydnney:
Ahoj. Nejsem chemik a veličina molární kapacita vody je mi cizí. Ale chybu očekávám v tomto: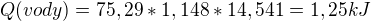
Tady počítáš teplo, které musela voda o hmotnosti m přijmout při ohřátí od dané delta t. V tom vzorci je c jako měrná tepelná kapacita vody, která je c = 4180 J.kg^-1 K^-1. Dosazuješ tam něco jiného.
Ta tvá molární kapacita vody tam ani nevychází jednotkově. Abys jí mohla použít, musela bys na to mít nějaký vtah, který neznám, ale podle jednotky by asi vypadal nějak takto: 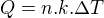 kde k (nevím jak se značí) je ta molární kapacita. Pak bys musela přepočítat i hmotnost vody na moly.
kde k (nevím jak se značí) je ta molární kapacita. Pak bys musela přepočítat i hmotnost vody na moly.
Offline
#4 21. 12. 2011 18:51
Re: spalné teplo anthracenu
↑ Sydnney:
Takže je to tak, jak jsem psal, nebo jinak? Docela by mě to zajímalo :-)
Offline