Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 07. 03. 2013 18:19
termochemia
Na základe termochemických rovníc:
a
vypocitajte mnozstvo tepla, ktore sa uvolni alebo spotrebuje pri odpareni jedneho molu H2O(l).
Prosim vas viete mi s tým niekto poradit, vysvetlit? Výsledok je okolo 44kJ.mol-1, takže jediné čo ma napadá je, že voda v plynnom stave ako keby nemala entalpiu, žiadnu energiu lebo inak si to neviem vysvetlit....ďakujem
Offline
- (téma jako vyřešené označil(a) Mary)
#4 07. 03. 2013 20:52
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: termochemia
Zdravím,
rovnice jsou téměř identické, jen v 1. rovnici je voda ve "stavu odpařeném", tedy ze stavu kapalného ještě přešla do plynného. Proto 1. rovnici zapíšeme  . A odečteme 1. rovnice minus 2. rovnice (nezapomenout, že počítáme teplo na 1 mol (a doufám, že jsem nepopletla znaménka :-), případně dejte vědět). Stačí tak? Děkuji.
. A odečteme 1. rovnice minus 2. rovnice (nezapomenout, že počítáme teplo na 1 mol (a doufám, že jsem nepopletla znaménka :-), případně dejte vědět). Stačí tak? Děkuji.
Offline
#5 09. 03. 2013 12:26
Re: termochemia
jelena napsal(a):
Proto 1. rovnici zapíšeme
.
Prečo 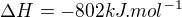 a nie
a nie 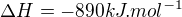 ?
?
A ešte otázka. Zo zadaných rozdielov entalpií vyplýva, že voda v plynnom skupenstve má väčšiu energiu (entalpiu) ako voda v kvapalnom skupenstve ? Alebo iba to, že na to odparenie sa spotrebovala energia ?
A keď to počítam, že 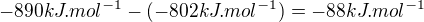 to platí pre 2 moly, takže pre jeden mol
to platí pre 2 moly, takže pre jeden mol  to je
to je 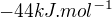 , no čo s tým mínuskom?Čo to znamená? Logicky prídem na to, že sa tolko energie sa spotrebovalo aby sa premenila voda na plyn, alebo sa nebodaj uvolni?
, no čo s tým mínuskom?Čo to znamená? Logicky prídem na to, že sa tolko energie sa spotrebovalo aby sa premenila voda na plyn, alebo sa nebodaj uvolni?
I tak moc díki, ale nemám v tom ešte veľmi jasno...tak budem rada ak by ste mohli pomôcť. Ďakujem
Offline
#6 09. 03. 2013 16:10
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: termochemia
↑ Mary:
děkuji, na možné nesrovnalosti ve znaménku jsem upozorňovala. -802, jelikož jsem upravovala 1. rovnici, kde bylo -802 (to se neměnilo, jen jsem nahrazovala H2O (gas).
Začnu od tohoto momentu:
Zo zadaných rozdielov entalpií vyplýva, že voda v plynnom skupenstve má väčšiu energiu (entalpiu) ako voda v kvapalnom skupenstve ? Alebo iba to, že na to odparenie sa spotrebovala energia ?
na odpaření vody z kapalného do plynného stavu je potřeba vynaložit energii, proto dle zákonu zachování energie voda v plynném stavu má větší energii, než v kapalném. Naopak při přechodu z plynného do kapalného stavu voda může tuto energii odevzdat.
1. reakce: 
říká, že vznik plynných produktů proběhl za vydělení tepla. Můžeme pokračovat v tom, že plynný produkt (vodu) necháme kondenzovat a získáme tak další teplo. A toto teplo jsem označila za "teplo odpařování" v první reakci (asi by bylo přehlednější, pokud bych k druhé reakci přepsala místo H2O (liquid) tak: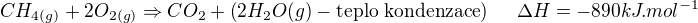
Zde význam "minus"teplo je stejný jako minus v 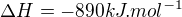 (tedy, že se také vylučuje). A první reakci nechala beze změny.
(tedy, že se také vylučuje). A první reakci nechala beze změny.
(1) 
(2) 
--------------------------------------------------
teď odečtením (1)-(2) dostaneme "teplo kondenzace", které se vyloučí při kondenzování 2 mol vody. Podělením 2 je teplo na 1 mol vody.
Je to tak lépe vidět? Děkuji.
Offline
#7 09. 03. 2013 18:55 — Editoval Mary (09. 03. 2013 18:57)
Re: termochemia
jelena napsal(a):
Je to tak lépe vidět? Děkuji.
Moc Díki. už to viem pochopiť. Ale ešte predsa niečo....
jelena napsal(a):
teď odečtením (1)-(2) dostaneme "teplo kondenzace", které se vyloučí při kondenzování 2 mol vody. Podělením 2 je teplo na 1 mol vody.
Tuna to víde vlastne kladné číslo(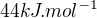 ), ale prečo keď ono sa to uvoľní?Vychádzam z tohto:
), ale prečo keď ono sa to uvoľní?Vychádzam z tohto:
jelena napsal(a):
Zde význam "minus"teplo je stejný jako minus v
(tedy, že se také vylučuje). A první reakci nechala beze změny.
Pochopila som to tak, že keď je mínus tak sa teplo uvoľnuje, no tuna vyšlo plus a aj tak sa uvoľnuje...
- - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - -
A ešte, kebyže chcem počítať priamo teplo ktoré sa spotrebuje pri premene vody v kvapalnom skupenstve na vodu v plynnom skupenstve, cize: 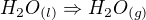
tak by sme to robili tak, ako ste to písali na začiatku ? :
jelena napsal(a):
Proto 1. rovnici zapíšeme
A odečteme 1. rovnice minus 2. rovnice.
Teraz tomu už chápem čo ste tým chceli povedať tym teplo odparovania a už ako to vlastne ste počítali i s tými premenami skupenstiev, no predsalen mám jednu otázku ešte. Ja by som nedala 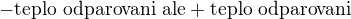 ciže
ciže 
A teraz kebyže odčítam (1.) mínus (2.) tak mi víde kladné čislo, vydelím a dostanem číslo, ktoré mi hovorí koľko energie treba dodať aby sa odparil 1 mol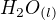 , nie?
, nie?
- - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - -
Je tu toho dosť a ani ja sa v tom už nevyznám tak zhrniem čo som sa chcela opýtať:
Keď to počítam podľa toho čo ste napísali naposledy(Váš posledný príspevok v tejto téme/ predošlý príspevok), dostanem plus 44 ale pritom sa počítalo teplo kondenzace(teplo sa vylučuje), tak nemalo by to byť minus 44 ?
Hádam tu som nepopísala úplne hlúposti (možno nad tým až zbytočne moc rozmýšľam) a znamienka (hlavne mínus ) nenávidím ....
Ešte raz díky...
Offline
#8 09. 03. 2013 19:46
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: termochemia
Code:
Pochopila som to tak, že keď je mínus tak sa teplo uvoľnuje, no tuna vyšlo plus a aj tak sa uvoľnuje...
už jsme to minus rovnou napsali, jelikož víme, že se uvolňuje, tedy ve výpočtu jsme dostali absolutní hodnotu tepla. A tu absolutní hodnotu stejně dobře můžeme použit jako teplo odpařování nebo teplo kondenzace. Znaménko u  se zavedlo jen "formálně", aby se rozlišilo, zda uvolňuje, nebo spotřebuje.
se zavedlo jen "formálně", aby se rozlišilo, zda uvolňuje, nebo spotřebuje.
Také jsme mohli napsat s (+teplo), že znaménko nevíme a podle výsledného znaménka usuzovat, zda se uvolní, nebo naopak spotřebuje.
A ešte, kebyže chcem počítať priamo teplo ktoré sa spotrebuje pri premene vody v kvapalnom skupenstve na vodu v plynnom skupenstve, cize:
jelikož to je jediná přeměna, o kterou se liší reakce (1) a reakce (2), tak to můžeš počítat rovnou a to 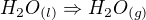 ,
, 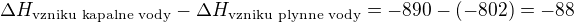
a v tom je přesně vidět, že při vzniku "kapalné" vody z "plynné" se teplo uvolní, což OK, jelikož se uvolní při kondenzaci vody.
Princip odečtu reakcí od sebe jsem použila, jelikož se tak v tomto typu úloh používá a je dost přehledný (i v případě více uvažovaných reakcí a více změn). Případně se ještě ozvi, pokud něco není jasné.
Offline
#9 09. 03. 2013 21:36
Re: termochemia
Zdravím v tématu,
Celkem dost dobře použitelný je tu Hessův trojúhelník.
Jinak něco k entalpii:
Entalpie je neměřitelná veličina shrnující mnoho údajů o dané molekule - kinetickou energii, rotační energii, potenciální energii, skupenství, atd. Nemůžeme přesně změřit hodnotu entalpie, můžeme ovšem měřit její změny. A tyto změny jsou tabelovány pro jednotlivé reakce jako (delta)H.
Doučím M, Ch v okolí Pardubic
Press any key to continue. Alt + F4?
Offline


