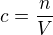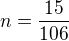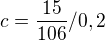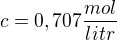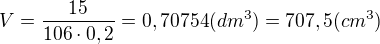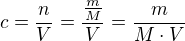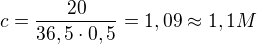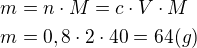Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 26. 04. 2009 19:39
rovnice molarni koncentrace
prosim o pomoc s temito priklady. par sem jich uz vypoctala,ale nevim si vubec rady s temito.
1, Jaky objem 0,2 molarniho roztoku Na2CO3 muzeme pripravit z 15 g teto slouceniny? Mr(Na2CO3) = 106
2, V O,5 dm3 roztoku je obsazeno 20 g chlorovodiku. Jaka je molarita teto kyseliny?
3, Kolik gramu NaOH je obsazeno ve 2 dm3 jeho 0,8 molarniho roztoku?
4, Kolik cm3 66% kyseliny dusicne je treba na pripravu 3 dm3 5 molarniho roztoku teto kyseliny?
Mr(HNO3) = 63,0 , hustota = 1,40 g.cm -3 = 1400 g/dm3
5, Kolik gramu NaCl obsahuje 1cm3 1,1 molarniho roztoku teto latky?
1, 707,5 cm3
2, 1,10 M
3, 64 g
4, 1022,7 cm3
5, 6,4.10-2
C= n/V
Moc prosim o pomoc
Offline
#3 26. 04. 2009 19:54
- Pavel Brožek


- Místo: Praha
- Příspěvky: 5694
- Škola: Informatika na MFF UK
- Pozice: Student
- Reputace: 194
Re: rovnice molarni koncentrace
↑ Alivendes:
2) Pokud si dobře ze střední pamatuji, tak x molární roztok existuje (ve smyslu, že jeho koncentrace je x mol/dm^3). V čem je problém?
Offline
#5 26. 04. 2009 20:31 — Editoval O.o (26. 04. 2009 20:34)
Re: rovnice molarni koncentrace
↑ aaaninka:
Ahoj -),
nejsem žádný odborník, jen tak to zkouším, snad se do výsledku trefím. Jednotku ti tu udělal Alivendes, zbytek je variace dvou vzorců (viz. níže).![kopírovat do textarea $ M=\frac{m}{n} \ [g \cdot mol^{-1}] \nl C=\frac{n}{V} \ [mol \cdot dm^{-3}] $](/mathtex/6c/6c4570f9bca85cd631a62c9db3d28aef.gif)
Někde se dává jednotka C jako M, respk. 1M, myslím, že jsem tu už někde viděl, ale kdo ví -).
Molární hmotnost jsem střihnul jen odboku z hodnot co si pamatuji, na přesnější si musíš najít tabulku mne už půl hodinky utíkají Vraždy v Midsomeru ;-).
2)
Obdobně řeš i další příklady, vychází to vše pěkně..
EDIT: Ty indexy trochu kazí strukturu, tak jsem je ve vzorcích smazal, ale je asi jasné o co jde, že?
EDIT II: Kolega výše má pravdu, tohle moc matematický problém nepřipomíná ;-).
Offline
#7 26. 04. 2009 21:13 — Editoval O.o (26. 04. 2009 21:19)
Re: rovnice molarni koncentrace
↑ aaaninka:
Rychle rychle jsou reklamy, snad to nezpletu:
Snad je tohle možné použít ;-)..
PS: Tuším, že tu hustotu použij až na konec řešení, nejprve zjisti hmotnost a pak už to jen podělíš hustotou..
Offline
#8 26. 04. 2009 21:27
Re: rovnice molarni koncentrace
Nejsem učitelka, proto matematiku neučím, ale přímo ji řeším...
Offline
#12 26. 04. 2009 22:19
Re: rovnice molarni koncentrace
↑ gadgetka: dekuju moc, uz to mam vypocitane... opravdu moc ste mi pomohli, dekuji
Offline
#13 26. 04. 2009 22:28
Re: rovnice molarni koncentrace
↑ aaaninka:
Jsi geniálnější jak já. Takhle jsi to vyřešila velmi pěkně. Nakonec oblíbený vzorec o kterém jsem psal je nahrazen trojčlenkou .. je to běžné často bývá možnost počítat to trojčlenkou nebo vzorcem, obojí vede ke stejnému cíli (jsem nadšený, že jsi prokoukla v zadání ten převod hustoty). Kdyby bylo něco třeba, tak se znovu ozvy, gadgetka (zdravím) se ani nestihla na těchto příkladech pořádně zahřát =).
Offline