Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#3 12. 04. 2015 21:06
Re: Změny skupenství látek 4
↑ Brzls: Zjistil jsem si tedy, že molární hmotnost vodní páry je 18 (H=1, O=6 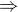 H2O = 18) a že molární plynová konstanta je 8,31. Hustotu vodní páry jsem našel jen z internetu z 1 zdroje (takže je to pochybné) a to: 0,5977 kg m−3 . Po vyjádření tlaku a dosazení do tvé rovnice mi vyšlo 82,78 Pa, ale podle výsledků v učebnici by to mělo vyjít 13 kPa. Poradil bys mi prosím, kde jsem udělal chybu? Děkuju moc.
H2O = 18) a že molární plynová konstanta je 8,31. Hustotu vodní páry jsem našel jen z internetu z 1 zdroje (takže je to pochybné) a to: 0,5977 kg m−3 . Po vyjádření tlaku a dosazení do tvé rovnice mi vyšlo 82,78 Pa, ale podle výsledků v učebnici by to mělo vyjít 13 kPa. Poradil bys mi prosím, kde jsem udělal chybu? Děkuju moc.
Offline
#4 12. 04. 2015 21:51
Re: Změny skupenství látek 4
↑ David7:
Hustotu v žádných tabulkách nehledej, to je blbost. Máš zadaný objem a máš zadanou hmotnost. Jak tedy spočítáš hustotu?
A pozor na tu molární hmotnost, aby si jí měl ve správných jednotkách
Offline
#5 12. 04. 2015 22:12 — Editoval mesikek (12. 04. 2015 22:14)
Re: Změny skupenství látek 4
Ahoj. Omlouvám se, že to tu píšu jakoby znovu, ale chtěl bych, aby kolega pochopil, o co zde jde. Evidentně totiž vůbec netuší, o co jde. :-) (takže si jsem vědom, že zde píšu to samé podruhé)
Vycházíš ze stavové rovnice ideálního plynu. 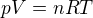
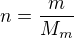
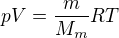
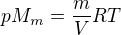
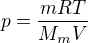
Pozor - platí následující - 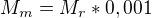 - což znamená, že molární hmotnost vodní páry bude 0,018. Po dosazení do
- což znamená, že molární hmotnost vodní páry bude 0,018. Po dosazení do 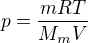 Ti vyjde správný výsledek.
Ti vyjde správný výsledek.
Závěrem jen připomenu, že je potřeba převést stupně Celsia na Kelviny. 0°C=273,15 K
A máš vyřešeno. :-)
Offline
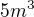 se nachází přehřátá vodní pára o hmotnosti 0,25 kg a teplotě 300°C. Jaký tlak má tato pára?
se nachází přehřátá vodní pára o hmotnosti 0,25 kg a teplotě 300°C. Jaký tlak má tato pára?