Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#2 20. 10. 2015 22:33
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: mol. koncentrace, molalita, molární zlomek
ano, předpokládáš dobře, můžeš určit n=m(Na2CO3)/Mr(Na2CO3), můžeš určit 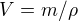 (roztoku). A už bys měla dopočíst všechno.
(roztoku). A už bys měla dopočíst všechno.
A děkuji za "děkuji" v jiném tématu.
Offline
#4 20. 10. 2015 23:08 — Editoval jelena (20. 10. 2015 23:09)
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: mol. koncentrace, molalita, molární zlomek
↑ klokie:
ne, mluvíme o objemu roztoku, jehož hmotnost byla 100 g, tedy V=100/1,135 (ml). Látkové množství n se vztahuje k rozpuštěné látce, proto n=13/Mr(Na2CO3). Ale objem se vztahuje k roztoku, jehož charakteristiky počítáš. Zbytek už podle vzorců. Jen si promyslí pořádně začátek výpočtu, zdárné dokončení přeji.
Offline
#5 21. 10. 2015 09:27
Re: mol. koncentrace, molalita, molární zlomek
↑ jelena:
Aha, ano. Mohu se pro jistotu zeptat na výsledky,
molární koncentrace je tedy: c=n/V = 0,15/88,1ml=1,72 mol/l?
molalita= n/m= 0,15/13 = 0,01 mol/g?
a u toho molárního zlomku mám dosadit co jako druhé n?...
předem děkuji :)
Offline
#6 21. 10. 2015 12:48
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: mol. koncentrace, molalita, molární zlomek
↑ klokie:
Zdravím,
n=13/Mr(Na2CO3) snad by mělo být o něco přesněji, než 0,15 - jak jsi dosazovala? Potom vzorec pro molární koncentraci OK, dosazování dobře (jen zkontroluj 0,15).
Molalita - souhlasí definice (látkové množství rozpuštěné látky na hmotnost rozpouštědla) co je u Tebe 13 g a kde je hmotnost rozpouštědla, když roztoku bylo 100 g? Ještě podle vašeho materiálu zkontroluj jednotky (mol/g, nebo mol/kg).
Molární zlomek - opět souhlasí definice? V jmenovateli je součet látkových množství složek směsí, směs je tvořena Na2CO3 a vodou. Podaří se dokončit? Děkuji a zdary.
Offline