Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 15. 10. 2016 11:40
stavová rovnice ideálního plynu
Zdravím,
Nevím si rady s touto úlohou na stavovou rovnici ideálního plynu:
Horkovzdušný balón má hmotnost 480 kg. Vypočtěte, na jakou průměrnou teplotu se musí ohřát vzduch v balónu o objemu 2500 m3, aby balón vzlétl. Okolní vzduch má teplotu 16°C, hodnota atmosférického tlaku je 1005 hPa (pro zjednodušení předpokládejte, že tlak v balónu je stejný jako tlak v okolí).
m1=480 kg
t1 = ?
t2 =16°C
p = 100500 Pa
M = 28,83 g/mol (molární hmotnost vzduchu, kterou můžeme používat, jinak by to prý mělo jít bez dohledání dalších hodnot)
vzhledem ke konstantnímu tlaku jsem se vydělením rovnic dostal na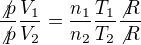
resp. 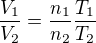
a nevím co s tím dál, protože objem okolního vzduchu dostat nemůžu a neznám hmotnost vzduchu v balónu na výpočet látkového množství
Díky za všechny rady
Offline
- (téma jako vyřešené označil(a) 2pir)
#2 15. 10. 2016 18:21
Re: stavová rovnice ideálního plynu
Nejprve stavovou rovnici vypočítáme hmotnost okolního vzduchu o objemu, rovném objemu balonu. Látkové množství n nahradíme poměrem m/M a molární hmotnost dosadíme v kg/mol:
p*V = n*R*T=> n = p*V/(R*T) => m/M = p*V/(R*T) => m = p*V/(R*T*M)
m = 100500*2500/(8,3145*289,15*0,02883) = 3624,95kg je hmotnost vzduchu o stejném objemu, jako má balon při teplotě 16°C = 289,15K a tlaku 100500Pa
Hmotnost teplého vzduchu v balonu musí být nejméně o 480kg menší. Stavovou rovnici poněkud upravíme. Tlak, objem, molární hmotnost a molární plynová konstanta se nemění. Hmotnost teplého vzduchu v balonu je o 480kg menší: m1 = m - 480 = 3624,95 - 480 = 3144,95kg. Ze stavové rovnice dostaneme:
p*V =( m/M)*R*T => m*T = p*V*M/R = m1*T1 => T1 = m*T/(m-480) = 3624,95*289,15/3144,95 =
= 333,21K = 60,06°C.
OK?
Offline
#3 15. 10. 2016 19:14
#4 15. 10. 2016 19:29
Re: stavová rovnice ideálního plynu
Všechno chápu a moc děkuji za vysvětlení.
Původně mě nenapadlo, jak zjistit hmotnost vzduchu, protože jsem neznal objem.
P.S. Hned v prvním řádku výpočtu je chyba ve vyjádření hmotnosti (molární hmotností se násobí), takže to vyjde cca 70,8°C
Offline