Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 27. 11. 2016 18:47
Chemické reakce (rovnice)
Dobrý den,
prosím Vás, potřeboval bych poradit ohledně chemických reakcí.
Kyselina bromovodíková + Oxid cínatý ->>>
Co bude vznikat?
HBr + SnO ---> ???
b) měl bych dotaz obecně, jak vždy poznám, co vůbec bude vznikat, dělám nyní příklady na procvičování a přijde mi, že to musím umět vysvloveně nazpaměť, třeba proč:
Sodík a voda vzniká: Na + H2O ---> NaOH + H2 a ne NaO + H2?
Jaká je pomůcka, jak zpaměti a prostě z hlavy rozpoznat, co vznikne u jakékoliv reakce? Díky
Offline
#2 27. 11. 2016 19:21
Re: Chemické reakce (rovnice)
a) Reaguje kyselina s amfoternym oxidom, ktory sa teda bude spravat ako zasada a takuto reakciu urcite poznas. Skus sam napisat, co vznikne.
b) Niektore veci sa proste musis naucit naspamet a naucis sa to len casom a praxou. Patri k tomu napriklad aj to, ze sa naucis, ktore oxidy su kysle, amfoterne a zasadite ako v a). Dalsim prikladom mozu byt reakcie manganistanu v kyslom, neutralnom a zasaditom prostredi. To je taky bezny skolsky priklad, ktory ked si par krat vyskusas, budes v buducnosti vediet. K otazke: alkalicke kovy vo vode tvoria hydroxidy, oxid nemoze vznikat, lebo ten je silne alkalicky a ihned by reagoval s vodou a vznikal by znova hydroxid.
Offline
#3 27. 11. 2016 19:33
Re: Chemické reakce (rovnice)
Jinak mohu ještě dotaz? Ostatní reakce si myslím že v pohodě - vždy je pravidlo - nemění se oxidační čísla...
Ale tady je zadání, které mě trochu mate a internet mi potvrdil totéž, ovšem nevím, jak to odvodit.
c) Síran hlinitý + měď
Al2(SO4)3 + Cu ---> Zde jsou oxidační čísla u hliníku III, Síran -II, měď
---> má vznikat CuSO4 + Al, hliník je jasný jen mi není jasná ta měď. Když má ve výchozím kroku 0 oxidační číslo, tak jak může přejít v oxidační číslo II? Tzn. že nevznikne Cu2SO4 , jak jsem myslel, ale vznikne síran měďnatý, tedy CuSO4 ... Jaktože zde se oxidační číslo mění a celkově, jak to poznám? Mě by třeba nenapadlo že tady se ox. číslo bude měnit a já bych napsal prostě dle pravidel to Cu2SO4...
Díky
Offline
#4 27. 11. 2016 19:47
Re: Chemické reakce (rovnice)
To samé tady - význam a podstatu vzniku reakce chápu, ale díky oxidačnímu číslu, které se tu opět změní, což nevím proč, tak vznikne vlastně něco jiného:
d) Mangan + Kyselina chlorovodíková
Jak se říká, čím jednodušší, tím složitější věda (pro mě to platí) tato reakce je primitivní, ale chci tomu rozumět opravdu díky všem detailním krokům, v tomto příapdě díky oxidačnímu číslu...
Mn + HCl --->
Mn má 0, H +I, Cl -I.... vzniká ---> MnCl + H2 takto by to napadlo mě...
Ale má vzniknout MnCl2 + H2 tím pádem ale nevím, proč mangan změnil oxidační číslo z 0 na 2 že místo MnCl původního vzniklo MnCl2 - tedy chlorid managanatý...
Offline
#5 27. 11. 2016 19:50
Re: Chemické reakce (rovnice)
Tak tato reakcia nebude urcite prebiehat. Bude prebiehat presne opacnym smerom. Ked sa nad tym zamyslis, preco by uslachtila med reagovala so solou neuslachtileho kovu? Preco by mala med vytlacit hlinik zo svojej soli? Preco by med mala odovzdat svoje elektron/y ked ona je stastna v oxidacnom stave 0? :D Na tuto tematiku si pozri Beketov rad kovov a pochopis to, preco tvoja rekacia nemoze fungovat. Plus ked chces maly bonus a bol tu spomenuty hlinik, pozri si nieco o aluminotermii :)
Offline
#6 27. 11. 2016 19:55
Re: Chemické reakce (rovnice)
↑ Kenniicek:
Dobře, ale neřeším tady pořadí reakce - tzn. jestli bude opačným či neopačným směrem, takto bylo zadání v příkladech, spíše se bavím o změně oxidačního čísla ... proč?
Offline
#8 27. 11. 2016 19:56
Re: Chemické reakce (rovnice)
Toto je docela extrém, tohle bych neodvodil snad nikdy....
Jak to bude, prosím a jak postupovat?
Hydroxid výpenatý + Oxid dusičný ---> ...
Ca(OH)2 + N2O5 ---> ???
Má prý vzniknout Ca(NO3)2 + H2O to tedy nevím, kde vzít :D
Offline
#9 27. 11. 2016 20:03
Re: Chemické reakce (rovnice)
↑ DTBChemie:
Zdravím.
Mangan se většinou v oxidační čísle I nevyskytuje. Nejčastější oxidační číslo u sloučenin manganu jsou II, IV, VI a VII, popřípadě se můžete setkat i s manganem v oxidačním čísle III a V, zbylá už nejsou tak běžná. Oxidační číslo II je velmi stabilní.
S něčím obdobným se setkáte například i u železa. Když rozpouštíte železo v HCl, vzniká chlorid železnatý (nikoliv železný). U železa se nejčastěji vyskytují oxidační čísla II a III, přičemž železité soli vznikají oxidací železnatých solí. Tedy pokud byste chtěl vyrobit chlorid železitý, musel byste k HCl přidat oxidační činidlo, např. peroxid vodíku, a až pak v ní to železo rozpustit. Pokud ale železo rozpouštíte v kyselině dusičné, vzniká dusičnan železitý, protože HNO3 je kyselina s oxidačními účinky. Jak už zde výše zmiňoval kolega ↑ Kenniicek:, některé věci se musíte naučit nazpaměť. Chce to jen cvik a praxi.
K tomu síranu hlinitému s mědí. V reálu by tato reakce ani neběžela, protože hliník stojí v Beketovově řadě kovů před mědí. Hliník by mohl vytěsnit měď ze síranu měďnatého ne naopak. Každopádně měď při reakcích upřednostňuje oxidační stav II. Měďné soli se připravují redukcí měďnatých solí.
Offline
#10 27. 11. 2016 20:06
Re: Chemické reakce (rovnice)
↑ DTBChemie:
Oxid dusičný se ve vodě rozpouští za vzniku kyseliny dusičné. Pokud reaguje kyselina s hydroxidem, jedná se o neutralizaci - proto ten dusičnan vápenatý a voda.
Offline
#11 27. 11. 2016 20:25
Re: Chemické reakce (rovnice)
↑ Bedlasky:
Děkuji mnohokrát, sice nevím, jak poznat, že bude vznikat kyseliny dusičná?, ale o.k. :-)
Ještě mohu dotaz tady prosím? Přijde mi to jako složitá reakce:
Kyselina dusičná + sulfid olovnatý =>
HNO3 + PbS ---> Má prý vznikat 2 H2O + 2 NO2 + Pb(NO3)2 + S popřípadě (8 HNO3 + 3 PbS = 4 H2O + 2 NO + 3 Pb(NO3)2 + 3 S)
Jakto? respektive jak vědět že vznikne tolik jednotlivých sloučenin a prvků? Děkuji moc
Offline
#12 27. 11. 2016 22:52
Re: Chemické reakce (rovnice)
↑ DTBChemie:
Jak to? Protože Latimerovy a Frost-Ebersovy diagramy, protože složitá soustava redoxních potenciálů. Každá redoxní reakce má přiřazený nějaký potenciál, když se dvě sloučeniny, které mohou podstoupit redoxní reakci (jedna z látek se pak bude oxidovat, druhá redukovat), sejdou, podle potenciálů se určí, jak ochotně bude reakce probíhat.
Jednodušeji: Když si napíšeme jen iontovou reakci, tak pak vidíme toto: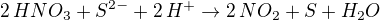
Toho zas tolik není, ne? Ty ostatní věci, co máte v reakci, na sebe jen "zbyly". (Rozhodně nelze dusičnan olovnatý považovat za zásadní produkt této redoxní reakce, je to jen "odpad")
Doučím M, Ch v okolí Pardubic
Press any key to continue. Alt + F4?
Offline
#13 28. 11. 2016 00:22
Re: Chemické reakce (rovnice)
↑ houbar:
Děkuji, zkusím se na to nějak podívat. Kažopádně ještě prosím odpověď k té reakci
Jak lze tohle jen tak z hlavy vědět, že vznikne tolik sloučenin?
a ještě mám dotaz k této reakci...
*) oxid fosforečný + oxid barnatý
P2O5 + BaO ---> vznikne Ba3(PO4)2 fosforečnan barnatý, svým způsobem chápu, že vzniká kyselina fosforečná, ale nevím, proč a jak to odvodit spojením prvků a oxidačních čísel...
Jak postupovat při takové rekaci se vznikem fosforečnanu barnatého? Jak si to odvodit, protože když bych chtěl jakože logicky spojit ionty, tak to fosforečnan barnatý nevyjde. Jak tedy poznám (klidně i mezikroky) že vznikne právě fosforečnan barnatý...
Offline
#14 28. 11. 2016 00:23 — Editoval Bedlasky (28. 11. 2016 00:24)
Re: Chemické reakce (rovnice)
↑ DTBChemie:
Kyselinotvorné oxidy se ve vodě rozpouští za vzniku kyselin (např. CO2, P4O10, NO2, SO2, SO3 atd.), zásadotvorné oxidy se ve vodě rozpouští za vzniku hydroxidů (např. Na2O, K2O, Li2O, BaO, CaO atd.).
Co se týče toho, jak určit co vzniká, někdy je to o intuici, někdy to prostě víte, protože jste se s tím setkal nebo to určíte podle vlastností látek. Časem na to získáte dobrý odhad, ač kolikrát člověk musí zapátrat na internetu.
Offline
#15 28. 11. 2016 00:36
Re: Chemické reakce (rovnice)
↑ Bedlasky:
Dobře, děkuji :-)
Mohu ještě dotaz, prosím, ohledně reakce
oxid fosforečný a hydroxid barnatý
P2O5 + Pb(OH)2 --->
Já bych řekl, že vznikne Pb3(PO4)2 + H2O, ale internet říká něco jiného nebo vůbec nic.
Co tedy vznikne a proč a jakým způsobem (krokem)
Offline
#16 28. 11. 2016 00:49
Re: Chemické reakce (rovnice)
↑ DTBChemie:
Ano, máte pravdu. Oxid fosforečný je kyselinotvorný oxid, hydroxid olovnatý je zásada, jedná se o neutralizaci.
Offline
#18 28. 11. 2016 01:12
Re: Chemické reakce (rovnice)
A rád bych prosím ještě nechal si vysvětlit tuto rovnici:
Fe + H2SO4 = Fe2(SO4)3 + H2
Proč nevzniká FeSO4 ? Tedy železnatý, ne železitý. železitý by mě třeba nenapadnul a jak to tedy poznám, že vznikne železitý?
Offline
#19 28. 11. 2016 01:45 — Editoval Bedlasky (28. 11. 2016 01:48)
Re: Chemické reakce (rovnice)
↑ DTBChemie:
Tak logicky. Oxid dusitý je kyselinotvorný oxid, oxid olovnatý je zásadotvorný oxidy - bude to neutralizace. Jak se jmenuje kyselina dusíku s ox. číslem III? A jak se jmenuje její sůl?
↑ DTBChemie:
Záleží na koncentraci kyseliny. Ve zředěné kyselině se rozpouští takto:
Na internetu jsem dohledal, že v koncentrované se ale rozpouští takto:
Je to dáno tím, že koncentrovaná kyselina sírová má oxidační vlastnosti, zatímco zředěná ne.
Offline
#20 28. 11. 2016 21:42
Re: Chemické reakce (rovnice)
↑ Bedlasky:
Děkuji, mohu ještě poprosit tu rovnici před žlutým příspěvekem?
Děkuji mnohokrát
Offline
#21 28. 11. 2016 21:48 — Editoval Bedlasky (28. 11. 2016 21:49)
Re: Chemické reakce (rovnice)
↑ DTBChemie:
Zkuste nad tím zauvažovat. Jaká kyselina dusíku má oxidační číslo III? Napište mi sem její vzorec. Pak budeme pokračovat dále. Musíte se to naučit odvodit sám, ve škole Vám nikdo nebude diktovat správné výsledky.
Offline

