Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 27. 01. 2017 14:16
- stereo-total-music
- Příspěvky: 213
Rovnovážná konstanta pro jednosložkový systém kapalina-pára
Ve skriptech na straně 17 je odvození BET izotermy.
Vůbec netuším, jak se přišlo na výraz pro rovnovážnou konstantu při kondenzaci páry do kapaliny: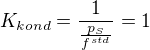
resp. jak lze tento výraz odvodit z podílu aktivit složky v plynné a kapalné fázi.
Nemáte někdo tušení?
Offline
#2 29. 01. 2017 10:08
Re: Rovnovážná konstanta pro jednosložkový systém kapalina-pára
↑ stereo-total-music:
Zdravím.
Aktivita kondenzovaných fází je z definice jednotková. (bavím se o čistých kapalinách a plynech, ne o roztocích)
To by mohlo pomoct.
Doučím M, Ch v okolí Pardubic
Press any key to continue. Alt + F4?
Offline
#3 29. 01. 2017 11:02
- stereo-total-music
- Příspěvky: 213
Re: Rovnovážná konstanta pro jednosložkový systém kapalina-pára
↑ houbar:
Ale nevím, jak je v tom vzorci vyjádřena aktivita plynné složky. Aktivita ideální plynné složky se nejběžněji vyskytuje jako: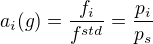
a tlak plynné složky nad kapalinou nemusí být roven tlaku nasycených par.
Offline
#4 29. 01. 2017 11:16
Re: Rovnovážná konstanta pro jednosložkový systém kapalina-pára
stereo-total-music napsal(a):
↑ houbar:
a tlak plynné složky nad kapalinou nemusí být roven tlaku nasycených par.
V tom případě ale systém není v rovnováze. (teda pokud to není vícesložkový systém)
Doučím M, Ch v okolí Pardubic
Press any key to continue. Alt + F4?
Offline
#5 29. 01. 2017 11:25 — Editoval houbar (29. 01. 2017 12:14)
- stereo-total-music
- Příspěvky: 213
Re: Rovnovážná konstanta pro jednosložkový systém kapalina-pára
↑ houbar:
rovnovážné adsorpce plynu do kapalné vrstvy na povrchu
Aha. Já myslel, že se bavíme o kondenzyci, tedy o fázovém přechodu pára-kapalina. Rozpouštění plynu v kapalině je ale jiný proces.
Obecně platí, že parciální rovnovážný tlak, který bude odpovídat zkoumanému plynu, který se má rozpustit, bude jeho molární zlomek v kapalné fázi kráte tlak nasycených par. To je Raoultův zákon.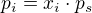
Pro některé plyny (většinou ty s nadkritickou teplotou), které se málo rozpouští, platí spíš Henryho zákon, kde je akorát jiná, semiempirická konstanta úměrnosti mezi molárním zlomkem v kap. fázi a tlakem nad ní.
Offline
#6 29. 01. 2017 12:41 — Editoval stereo-total-music (29. 01. 2017 12:42)
- stereo-total-music
- Příspěvky: 213
Re: Rovnovážná konstanta pro jednosložkový systém kapalina-pára
↑ stereo-total-music:
Nene uvažuje se, že adsorbovaná vrstva na povrchu adsorbentu je tenká vrstva jednosložkové kapaliny, takže je to rovnováha pára-kapalina, jestli to správně chápu. Proto mi nedává smysl, jak se v systému může vytvořit rovnováha kapalina-pára, když tlak plynu je obecně menší než tlak jeho nasycených par (adsorpce dusíku je provádí do tlaku jeho nasycených par za dané teploty).
Exaktnější odvození BETky vede asi přes kinetiku.
Offline
