Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 13. 03. 2017 12:31
1. termodynamické zákon
Ahoj, snažím se pochopit 1. termodynamický zákon, ale zasekla jsem se hned na začátku. Mohl by mi prosím někdo vysvětlit následující? Co znamená, když se řekne, že teplo je rovnomocné mechanické práci? Píší, že pod pojmem rovnomocné si lze představit vlastnost, kdy teplo a práce jsou si sice navzájem kvantitativně rovnocenné a lze je mezi sebou transformovat, ale přesto jsi nejsou rovnocenné kvantitativně. Nějak nerozumím, co si pod tím mám představit.
Děkuji za odpověď.
Offline
#2 13. 03. 2017 15:07
Re: 1. termodynamické zákon
Ten termín jsem nikdy předtím neviděl:-)
Ale podstata je, že z jakékoli "normální" energie můžeme teoreticky a často i prakticky bezeztrátově udělat tepelnou energii (např. ohřát vodu elektrickým topným tělesem, nebo ohřát dvě nepružná tělesa tím, že s nimi o sebe praštím), ale naopak to již principiálně nejde beze ztrát.
Převod z tepelné energie na "normální" obnáší zařízení, kterým teplo prochází a má tedy teplý a studený konec, přičemž k funkci je nutné, aby ze studeného konce nějaké teplo unikalo.
Podrobnosti viz Carnotův cyklus.
Offline
#3 13. 03. 2017 15:20
Re: 1. termodynamické zákon
↑ linet123:
Ahoj. V té větě co píšeš vidím za sebe logický spor, takže nevím. Je to nějak takhle. Ve fyzice se vyskytuje úžasná veličina - energie. Je to velmi abstraktní veličina a těžko odpovědět na otázku, co to vlastně je. Nicméně je velmi užitečná, protože se dá v mnoha situacích celkem snadno vypočítat a hlavně, za určitých okolností se zachovává. S kinetickou energií nebo potenciální energií v tíhovém poli ses jistě setkala.
V 1. TZ se vyskytují tři veličiny: vnitřní energie, teplo a práce. Vnitřní energie je součet "vzájemné" kinetické a vzájemné potenciální energie jednotlivých částic, ze kterých je dané těleso složeno. Teplo a práce mají popisovat změny energie. Když začnu těleso zahřívat, zvyšuje se kinetická energie těch částic, jako by se jistá energie přelévala z ohřívače na těleso. Tímto způsobem se přelévající energii se kdysi začalo říkat teplo. Pokud na těleso působím nějakou vnější silou a třeba ho zdeformuji (nebo lépe, mám plyn a ten stlačím, třeba nějakým písem), ohřeje se - vnitřní energie opět stoupla. (Mechanismus je u toho plynu takový, že částice se srážejí s pístem, který se ale pohybuje proti nim, a proto se odrazí s větší rychlostí, než měly předtím). Pokud k tomu nárůstu dojde takto, stoupne o stejnou hodnotu, jakou mechanickou práci vykonala ta vnější síla. Práce, teplo a vnitřní energie mají stejné jednotky (J).
A to je asi to podstatné, co říká 1. TZ. Tedy, pokud jsem měl soustavu v rovnovážném stavu, pak se něco stalo o ona dospěla do nového rovnovážného stavu s vyšší teplotou, muselo se to stát tepelnou výměnou s nějakým vnějším tělesem nebo konáním práce nějaké vnější síly. Nijak jinak to nejde a celkový nárůst vnitřní energie je roven součtu prvního a druhého vlivu. Vše samozřejmě za předpokladu, že mi do mé soustavy někdo něco nepřidal - musí to tedy být uzavřená soustava.
Shodou okolností se kolegové v jednom z vedlejších vláken zrovna teď pokoušejí rozhodnost, do jaké míry je to užitečné dělení, a do jaké míry je to blbá terminologie. Tak uvidíme na co přijdou. Z mých zkušeností není až takový problém, že se tam vyskytují tři pojmy pro popis něčeho podobného. Spíš se mnohdy klade důraz na terminologii (např. uzavřená / adiabaticky izolovaná / izolovaná / neizolovaná / otevřená soustava) a relativní detaily (např. znaménka u W a Q a nejrůznější kejkle s nimi), což pak odvádí pozornost od toho podstatného. Ale to je jen můj názor.
(V náhledu vidím edisonův příspěvek, ale tenhle tu nechám. Jednak jsem ho psal dlouho, jednak se mi zdá, že edison mluví spíš o 2. PT.)
Offline
#5 13. 03. 2017 16:43 — Editoval linet123 (13. 03. 2017 16:45)
Re: 1. termodynamické zákon
↑ edison:
↑ LukasM:
Děkuji za odpovědi :) Pomohly mi. Ještě bych se chtěla zeptat. Matematické vyjádření 1.T.Z. vypadá takto 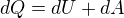 a dále i takto
a dále i takto 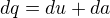 jaký je v tom konkrétně rozdíl? tuším že ve druhém vyjádření se jedná o měrné teplo, vnitřní energii a práci, ale nějak netuším proč se to tak vůbec může psát resp. kvůli čemu se to tak vůbec píše.
jaký je v tom konkrétně rozdíl? tuším že ve druhém vyjádření se jedná o měrné teplo, vnitřní energii a práci, ale nějak netuším proč se to tak vůbec může psát resp. kvůli čemu se to tak vůbec píše.
Děkuji.
Offline
#6 13. 03. 2017 18:23 — Editoval Ferdish (13. 03. 2017 18:25)
- Ferdish

- Zablokovaný
- Příspěvky: 4173
- Škola: PF UPJŠ (2013), ÚEF SAV (2017)
- Pozice: vedecký pracovník
- Reputace: 81
Re: 1. termodynamické zákon
Pokiaľ nie je definovaná konštanta alebo vzťah úmernosti medzi veličinami označenými rovnakým malým a veľkým písmenom (pričom musí byť identická pre každú dvojicu, aby ju bolo možné z výrazu krátiť), tak ide len a len o formálny prepis do malej abecedy.
Dôležité je, aby každý vedel, aká fyzikálna veličina je pod akým písmenom schovaná. Od toho je tu vyučujúci, učebnice, skriptá a ostatné učebné materiály.
Offline
