Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 06. 04. 2011 13:28
Tepelná kapacita, entalpie, entropie
Ahoj,
prosím o pomoc s výpočtem příkladů z fyzikální chemie.
číslo 3 jsem zde již našel z loňského roku a honděn mi to pomohloa ale ostatních pěti se moc nechytám. Stačilo by možná i "nahodit" jaký konkrétní vorec při výpočtech použít.
Offline
- (téma jako vyřešené označil(a) strom.tom)
#4 06. 04. 2011 16:08
Re: Tepelná kapacita, entalpie, entropie
Zdravím kolegu
U toho prvního příkladu se to počítá podle vzorce =suma koeficientů produktů - suma koeficientů reaktantů
=suma koeficientů produktů - suma koeficientů reaktantů
pro koeficient a (HBr) tedy bude platit 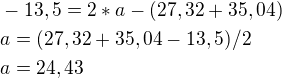
další koeficienty se dělají stejně
U druhého příkladu si musíš udělat rovnici pro hoření benzenu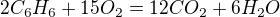
mělo by platit, že standardní spalná entalpie = sumě slučovacích entalpií produktů - suma slučovacích entalpií reaktantů
po dosazení
2*(-3274,1)=(-393,5-285,8)-2*x - kde x je slučovací entalpie benzenu
Třetí
pro změnu entropie platí  kde a= 293,15K a b=373,15K
kde a= 293,15K a b=373,15K
Radim, tedy jsem.
Dobrá rada je drahá, ta moje je zdarma.
Offline
#6 06. 04. 2011 23:24 — Editoval rleg (28. 06. 2011 08:36)
Re: Tepelná kapacita, entalpie, entropie
Čtvrtý
Pro tohle existuje jednoduchý vzorec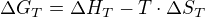
který se rozepíše do hnusného vzorce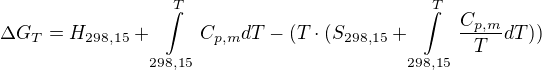
když to všechno dosadíš podle zadání a zintegruješ, budeš mít výsledek
Co se týče posledního příkladu, tam zatím nevím, jak se řeší.
Radim, tedy jsem.
Dobrá rada je drahá, ta moje je zdarma.
Offline
#8 12. 04. 2011 09:00 — Editoval františka21 (12. 04. 2011 09:05)
- františka21
- Zelenáč
- Příspěvky: 4
- Reputace: 0
Re: Tepelná kapacita, entalpie, entropie
Dobrý den,můžete mi pomoci,řeším jeden příklad jak jsem se dívala tak podobný už tady někdo poslal.
př. Při spálení 1g tuhého naftalenu (C10H8) v kalorimetrické bombě se při 291,15K uvolní 9621 cal tepla.Potřebuji vědět standartní slučovací entalpii naftalenu v KJ při teplotě 291,15K jsou li dány stanadrtní slučovací entalpie produktu spalné reakce naftalenu.
Molární hmotnost je 128,18g.mol-1
CO2 (g) -393,79KJ při teplotě 291,15K
H2O (l) -286,04KJ při teplotě 291,15K vím,že reakce je C10H8+12O (g)=10CO2 (g) +4H20 (l)
prosím o radu nějak nad tím sedím a nemůžu se dopočítat
díky
Offline
#9 12. 04. 2011 10:19
- františka21
- Zelenáč
- Příspěvky: 4
- Reputace: 0
Re: Tepelná kapacita, entalpie, entropie
Dobrý den,můžete mi pomoci,řeším jeden příklad jak jsem se dívala tak podobný už tady někdo poslal.
př. Při spálení 1g tuhého naftalenu (C10H8) v kalorimetrické bombě se při 291,15K uvolní 9621 cal tepla.Potřebuji vědět standartní slučovací entalpii naftalenu v KJ při teplotě 291,15K jsou li dány stanadrtní slučovací entalpie produktu spalné reakce naftalenu.
Molární hmotnost je 128,18g.mol-1
CO2 (g) -393,79KJ při teplotě 291,15K
H2O (l) -286,04KJ při teplotě 291,15K vím,že reakce je C10H8+12O (g)=10CO2 (g) +4H20 (l)
prosím o radu nějak nad tím sedím a nemůžu se dopočítat
díky
Offline
#10 12. 04. 2011 15:48 — Editoval rleg (12. 04. 2011 15:55)
Re: Tepelná kapacita, entalpie, entropie
↑ strom.tom: Zjistil jsem, že s tím tvojím posledním příkladem si nevím rady.
↑ františka21: Jestli jsem to pochopil správně, tak by se to mělo počítat zhruba takhle
Reakční entalpii naftalenu spočítáš z těch kalorií:  Mělo by vyjít zhruba -5150 kJ/mol
Mělo by vyjít zhruba -5150 kJ/mol
No a pak jen aplikuješ rovnici, že reakční entalpie = součtu slučovacích entalpií produktů - součet slučovacích entalpií reaktantů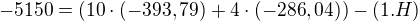
H mi vychází jako 68,21 kJ/mol
Radim, tedy jsem.
Dobrá rada je drahá, ta moje je zdarma.
Offline
#12 12. 04. 2011 20:42
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: Tepelná kapacita, entalpie, entropie
Zdravím vás,
pro 9. úlohu - zkuste projit příkladnik "Rovnovažné plynné směsí" a odkaz na vyjádření složení směsí.
5 mol % značí, že v rovnovažném stavu směs obsahuje 5 mol produktu (NH3) na 100 mol celkové směsi (zbytek (celkem velký) reaktantů, co nereagoval a produkt).
Je třeba sestavit latkovou bilanci - podle reakce (víme, že z 1 mol N2 vzníká 2 mol NH3, z toho plyne, jaká část N2 reagovala, zbytek je v rovnovážné směsi v původním stavu a nereaguje). Obdobně pro H2.
Mám prosbu - váše kolegyňky v minulém roce poskytly vaši sbírku (materiály k fyzikální chemie), byla by možnost opět ke stažení? Odkaz už není funkční.
A ještě prosba - dodržujte, prosím, pravidlo o jedné úloze do tématu, je to potom více přehledné. Jinak z vašeho tématu mám radost :-) Děkuji.
Offline
#13 13. 04. 2011 09:24 Příspěvek uživatele strom.tom byl skryt uživatelem strom.tom. Důvod: chyba
#14 13. 04. 2011 09:29 Příspěvek uživatele strom.tom byl skryt uživatelem strom.tom. Důvod: chyba
#18 13. 04. 2011 19:45
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: Tepelná kapacita, entalpie, entropie
↑ strom.tom:
Také děkuji.
Sbírku úloh, bohužel, nemám, proto jsem prosila někam umístit, pokud je možnost. Děkuji.
Offline
#19 18. 04. 2011 15:55
Re: Tepelná kapacita, entalpie, entropie
↑ jelena:
Odkaz by měl fungovat tento. Právě jsem jej vyzkoušel.
http://www.fmmi.vsb.cz/cs/okruhy/studiu … chemie.pdf
Offline
#20 18. 04. 2011 16:38
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: Tepelná kapacita, entalpie, entropie
↑ strom.tom:
Děkuji :-) To je jen pro vyvolené. Nevadí, měj se hezky.
...
Offline




