Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 18. 10. 2008 10:55
Plyn- teplo
Zdravím potřeboval bych poradit s následujícím příkladem:
Dva moly ideálního plynu teploty 300K byly nejprve izochoricky ochlazeny, přičemž se tlak plynu změnil na polovinu. Potom plyn izobaricky expandoval, až dosáhl původní teploty. Určete celkové množství tepla, pohlceného plynem při obou procesech?
Výsledená rovnice by měla být Q=(1/2) . n . R. T1
pozn. p . V = n . R . T(ideální plyn) Q= n . (3/2) . R . (T-T0) (izochor.)
Q= n . (3/2) . R . (T- T0) + p . (V- V0) (izobar)
Zkoušel jsem to dát dohromady z rovnic pro ideální plyn a izobarický a izochorický děj...ale
nezdařilo se:(....diky
Offline
#2 18. 10. 2008 13:55 — Editoval rughar (18. 10. 2008 13:58)
Re: Plyn- teplo
Teplota plynu byla stejná na začátku i na konci. Tím pádem má plyn shodnou celkovou tepelnou energii (Q). Výsledná změna tepelné energie je tedy Q = 0.
Něco jiného je celková energie plynu. Energie má totiž dvě složky. Tepelnou a vnitřní. Vnitřní energie se změnila, nebo? při izobarické expanzi se konala práce, kterou lze popsat jako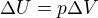
Na začátku izobarické expanze byl objem roven V0 (původní objem) a tlak byl po celou dobu nemění a to 1/2 * p0 (p0 = počáteční tlak). Lze tedy psát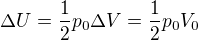
Nebo? změna objemu je rovna původnímu objemu (objem se zdvojnásobil). Ze stavové rovnice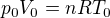 plyne, že
plyne, že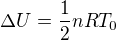
, kde T0 je původní teplota 300K. To je tedy výsledná energie, o kteru jsme plyn zahřáli o on nám to vrátil v podobě vykonané práce.
1 + 1 = 1 + 1
... a nebo taky ne
Offline
#3 18. 10. 2008 15:36 — Editoval BrozekP (18. 10. 2008 15:40)
- Pavel Brožek


- Místo: Praha
- Příspěvky: 5694
- Škola: Informatika na MFF UK
- Pozice: Student
- Reputace: 194
Re: Plyn- teplo
↑ rughar:
Co myslíš "celkovou tepelnou energií Q"? Teplota plynu je stejná, takže má na počátku a na konci stejnou vnitřní energii U. Změna vnitřní energie je nulová 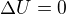 . Pak už mi není vůbec jasné, co myslíš "celkovou energií plynu, která má dvě složky - tepelnou a vnitřní".
. Pak už mi není vůbec jasné, co myslíš "celkovou energií plynu, která má dvě složky - tepelnou a vnitřní".
Tvůj další postup výpočtu dokážu pochopit, pokud si nahradím tvé  za práci
za práci  . Protože se vnitřní energie nezměnila, tak všechno teplo Q, které systému dodáme se přemění na práci, kterou jsi spočetl, tvůj výsledek je tedy s touto záměnou pochopitelný.
. Protože se vnitřní energie nezměnila, tak všechno teplo Q, které systému dodáme se přemění na práci, kterou jsi spočetl, tvůj výsledek je tedy s touto záměnou pochopitelný.
Uvedu i celé řešení, jak by se to dalo také dělat bez práce W:
Děj označím pomocí stavů 1 -> 2 -> 3, stavové veličiny pak příslušnými indexy. Pro dodaná tepla platí
Celkové dodané teplo je tedy (s využitím Mayerova vztahu)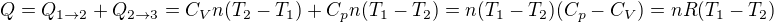
Porovnáme stavovou rovnici ideálního plynu ve stavech 1 a 2, dostaneme tak
a tedy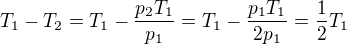
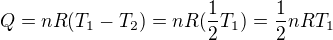
Offline
#4 18. 10. 2008 17:46
Re: Plyn- teplo
Má chyba v konvenci. Omlouvám se. To co jsem označil jeko Q tak je ve skutečnosti U. A tedy jelikož vím, že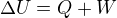
A zároveň změna vnitřní energie U zůstává neměnná. Pak platí, že dodané teplo Q je rovno práci, kterou plyn vykonal -W. Tedy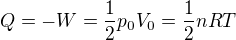
Takto měl vypadat můj postup, který vedl přes práci. Omlouvám se za vyjadřování (nemělo by se mi to stávat, když mám termodynamiku právě zapsanou jako předmět :-X)
1 + 1 = 1 + 1
... a nebo taky ne
Offline