Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#2 27. 11. 2013 13:46
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: Vyčíslování redoxních rovnic
Zdravím,
jelikož jde o celkem nezákeřné rovnice, snad by stačily odkazy úvodního tématu (nebo jiné dostupné materiály - co používáte?) Zkus, prosím, vypsat Tvé postupy, ať je vidět, proč nefungují. Děkuji.
Offline
#3 27. 11. 2013 14:15
Re: Vyčíslování redoxních rovnic
U první rovnice jsem na chybu už přišel. Jde o mojí minimální zkušenost s komplexy, proto jsem pozapomněl, že zlato má mít náboj +1, nikoliv +2 - tím by byl kyanid zlatnatý neutrální a nemohl by se tam navázat draslík.
Nicméně, postup:
Au (0) -1e ------------> Au (+1) OX. | 4
O2 (0) +4e -----------> 2O (-2) RED. | 1
Výsledek:![kopírovat do textarea $4Au+8KCN+O_{2}+2H_{2}O \Rightarrow 4K[Au(CN)_{2}]+4KOH$](/mathtex/99/994fb63b16cd6f4f4a254e0f723012f3.gif)
Otázka:
4KOH
Chápu to správně, že výsledné koeficienty (v tomto případě 4 a 1) píšu vždy k produktům?
Můžou se tyto čísla dále měnit, při následném vyčíslování?
Jelikož ke kyslíku (který je ve sloučenině KOH) jsem napsal 1, ale dále jsem to číslo změnil, abych měl 4 draslíky.
Offline
#4 27. 11. 2013 14:28
Re: Vyčíslování redoxních rovnic
U druhé rovnice jsem přišel na to, že nedokážu přijít na správnost oxidačního čísla dusíku u: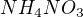
Pokud vím, že: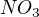 má náboj -1
má náboj -1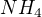 má náboj +1
má náboj +1
Vodík má náboj -1 v tomto případě. Vodíky jsou zde 4, tudíž celkově -4, my ale chceme výsledný náboj +1, takže dusík by měl mít +5. To je ale ovšem špatně, si myslím.
Offline
#5 27. 11. 2013 14:43
Re: Vyčíslování redoxních rovnic
A u poslední rovnice, kde mi mimochodem v zadání chybí:
Postup:
2I (-1) -2e ------------> I2 (0) | 6
Cr2 (+6) +6e ------------> 2Cr (+3) | 2
Ale správně by mělo být u chromu pouze +3e.
Tudíž nechápu, proč se v tomto případě nebere ohled na to, že na levé straně jsou dva chromy a na druhé straně pouze jeden. Je to z důvodu dimérních molekul?
Offline
#6 27. 11. 2013 16:33 — Editoval jelena (27. 11. 2013 16:35)
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: Vyčíslování redoxních rovnic
↑ Halfik:
děkuji. Pro shrnutí (i když pořádný materiál bude přínosnější) je tak, že zásadou je zákon zachování ve smyslu: počet elektronů přijatých je stejný jako počet elektronů odevzdaných a počet atomů každého prvku napravo je stejný jako počet atomů každého prvku nalevo. Toto dodržuješ při sestavení bilancí.
↑ 4 KOH:
|*4 znamená, že násobíš celou rovnici v bilančním řádku číslem 4, ovlivňuje to "základní prvky", co se účastnily samotného redox. procesu a vleče za sebou ovlivnění dalších prvků, co jsou se základními ve sloučenině. Proto nejdřív pomocí |*4 srovnám základní (Au) nalevo a napravo, potom odvozeně dorovnám prvky, co jsou ve spojení s Au a jsou jen v jedné sloučenině (CN) - dorovnám nalevo. Důvodem je, že toto dorovnání už neumím nijak ovlivnit.
Pokračují dorovnáním K, jelikož zde mám prostor napravo v KOH. Na závěr používám dorovnání H, O pomocí vody. A úplně na závěr ještě mohu použit jednoprvkové sloučeniny, jelikož tá nikoho jiného neovlivní. Zkus takto poskákat levo-pravo.
Jelikož ke kyslíku (který je ve sloučenině KOH) jsem napsal 1, ale dále jsem to číslo změnil, abych měl 4 draslíky.
měl jsi napsat 2 - viz elektronová bilance (ale zatím napíší slabým písmem, jelikož vím, že mohu potřebovat pro dorovnání K a nalevo mám prostor v osamoceném O2). O2 ještě není dorovnáno, třeba dokončit.
-------------------------------------------
↑ NH4:
NH4 - jednou jsi odvoď jak vzniká amonný kation (viz SŠ) a již se pamatuje, že je vždy NH4(+) a H v něm je (+), N(3-).
↑ Cr2O7:
2I (-1) -2e ------------> I2 (0) | 6
Cr2 (+6) +6e ------------> 2Cr (+3) | 2
Ale správně by mělo být u chromu pouze +3e.
u jednoho Cr jsou 3e přijaté, jelikož jsi urovnal počet atomu, tak celkem 6e. Ovšem řádek I bude vynásoben jen 3. Odsud 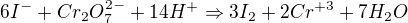
Tudíž nechápu, proč se v tomto případě nebere ohled na to, že na levé straně jsou dva chromy a na druhé straně pouze jeden. Je to z důvodu dimérních molekul?
Já bych zapsala tak, jak máš, ale je možná diskuse, zda striktně dodržovat dolní index _2 jako u O2, nebo 2 použit před Cr, že naznačuje počet atomů ve větší molekule. Ale i pokud napíšeš jen Cr, tak "budeš donucen" počty atomů dorovnat.
Můžou se tyto čísla dále měnit, při následném vyčíslování?
můžou se úměrně násobit a dělit stejným číslem nalevo a napravo za předpokladu zachování - viz úplně začátek mého příspěvku, to nemůžeš porušit.
Já pozoruji, že některé formy zápisů se mění (snad z nějakých metodických, nebo jinak opodstatněných důvodů), ale zákon zachování přetrvává.
Offline
#7 27. 11. 2013 18:21
Re: Vyčíslování redoxních rovnic
Děkuji za vyčerpávající odpověď. Už jsem se ty rovnice dopočítal a nejedna věc už mi je jasná.
Ale stále nedokážu pochopit:
u jednoho Cr jsou 3e přijaté, jelikož jsi urovnal počet atomu, tak celkem 6e. Ovšem řádek I bude vynásoben jen 3.
Kdy mám násobit dvojnásobným počtem elektronů a kdy ne.
Offline
#8 27. 11. 2013 18:28
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: Vyčíslování redoxních rovnic
↑ Halfik:
asi nerozumím úplně. Kdy máš napsat 2Cr.....Cr_2? Nebo proč
2I (-1) -2e ------------> I2 (0) | 3
Cr2 (+6) +6e ------------> 2Cr (+3) | 1
Offline

![kopírovat do textarea $Au+KCN+O_{2}+H_{2}O \Rightarrow K[Au(CN)_{2}]+KOH$](/mathtex/f9/f9aaae2f19b98984e2657fb2c5ad39be.gif)