Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 17. 06. 2016 00:48
- stereo-total-music
- Příspěvky: 213
Odvození Gibbsova fázového zákonu
Nechápu odvození Gibbsova fázového zákonu.
Mějme systém s 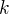 složkami v
složkami v 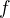 fázích v libovolném stavu (obecně mimo termodynamickou rovnováhu).
fázích v libovolném stavu (obecně mimo termodynamickou rovnováhu).
Každou fázi popisujeme teplotou, tlakem a složením:
Pro definici stavu systému stačí určit teploty, tlaky a molární zlomky  složek ve všech fázích (molární zlomek poslední složky ve všech fázích z toho již vyplývá). Celkem je tedy potřeba
složek ve všech fázích (molární zlomek poslední složky ve všech fázích z toho již vyplývá). Celkem je tedy potřeba 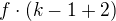 údajů.
údajů.
V termodynamické rovnováze nám stačí určit pro definici stavu systému:
1) Místo 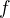 teplot pouze jednu teplotu, tedy o
teplot pouze jednu teplotu, tedy o 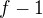 teplot méně.
teplot méně.
2) Místo 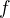 tlaků pouze jeden tlak, tedy o
tlaků pouze jeden tlak, tedy o 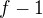 tlaků méně.
tlaků méně.
V termodynamické rovnováze je chemický potenciál  každé složky stejný ve všech fázích.
každé složky stejný ve všech fázích.
Při odvození počtu stupňů volnosti 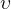 se postupuje následovně:
se postupuje následovně: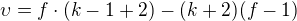
Z toho mi vychází, že místo chemického potenciálu složek ve všech fázích stačí určit pouze jejich potenciál v jedné fázi (jejich potenciály v ostatních fázích jsou stejné). Což platí v termodynamické rovnováze.
Nechápu však, jak z hodnoty chemického potenciálu složky 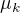 vyplývají její molární zlomky ve všech fázích. Může mi to někdo vysvětlit?
vyplývají její molární zlomky ve všech fázích. Může mi to někdo vysvětlit?
Offline
#2 18. 06. 2016 00:08
Re: Odvození Gibbsova fázového zákonu
↑ stereo-total-music:
Zdravim.
Pokud to nechcete s odvozením, tak platí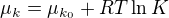
Doučím M, Ch v okolí Pardubic
Press any key to continue. Alt + F4?
Offline
