Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 07. 03. 2010 18:40
- pavlinkadivisova
- Zelenáč
- Příspěvky: 21
- Reputace: 0
10% peroxid
2K[Cr(OH)4] + 3 H2O2 + 2KOH=K2CrO4+ 8H2O
z týhle rovnice potřebuju spočítat 10% peroxid. vyšlo mi to, že mám 2,08356g H2O2
a 25,52ml vody, OK??????
ASpoň tohle je dobře?????
Offline
#2 07. 03. 2010 18:44
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: 10% peroxid
↑ pavlinkadivisova: máš tu rovnici dobře vyčislenou? Nezdá se mi to. Děkuji.
Offline
#3 07. 03. 2010 18:48 — Editoval pavlinkadivisova (07. 03. 2010 18:49)
- pavlinkadivisova
- Zelenáč
- Příspěvky: 21
- Reputace: 0
Re: 10% peroxid
2K[Cr(OH)4] + 3 H2O2 + KOH=2K2CrO4+ 8H2O
Offline
#4 07. 03. 2010 19:07
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: 10% peroxid
↑ pavlinkadivisova: asi už jen překlep.
2K[Cr(OH)4] + 3 H2O2 + 2KOH=2K2CrO4+ 8H2O
Prosím tebe, kdybys napsala postup, tak bych jen zkontrolovala a početně snad trojčlenka se nedá zkazit. Tak to musím celé počítat.
Kde jsme počítaly (my dvě) teoretické množství K[Cr(OH)4], co vzniklo v předchozí reakci a zde se používá jako vstup?
Offline
#5 07. 03. 2010 19:18
- pavlinkadivisova
- Zelenáč
- Příspěvky: 21
- Reputace: 0
Re: 10% peroxid
↑ jelena:není problém
takže z molární hmotnosti 0,0278*3= 0,0834, dále jsem to násobila 34, takže mi vyšlo 2,8356g peroxidu, z čehož jsem směšovačkou získala, že celkem mám 28,356- 2,8356= 25,52ml H2O
Offline
#6 07. 03. 2010 19:29
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: 10% peroxid
↑ pavlinkadivisova:
Máme 2,863 g Cr(OH)3, z předchozí reakce vypočtu, že vznikne 4,4196 g K[Cr(OH)4], toto dál vstupuje do reakce s peroxidem a potřeba čistého peroxidu je 1,418 g (což je polovina od tvého výpočtu).
Pokud počítaš přes mol, tak z 1 mol Cr(OH)3 vzniká 1 mol K[Cr(OH)4]), ale v reakci s peroxidem máme 2 mol K[Cr(OH)4] na 3 mol H2O2. Je to tak?
Offline
#7 07. 03. 2010 19:42
- pavlinkadivisova
- Zelenáč
- Příspěvky: 21
- Reputace: 0
Re: 10% peroxid
↑ jelena:
ok, užvím, kde je chyba...
a ještě poslední, spočtnout teoretický výtěžek K2Cr2O7
2K2CrO4 + 2 CH3COOH=K2Cr2O7 + CH3COOK +8 H2O
přes molární hmotnost , kterou násobím 294,19, mi vyjde 8,17g K2Cr2O7
Offline
#8 07. 03. 2010 20:01
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: 10% peroxid
↑ pavlinkadivisova:
opět nemáš dovyčisleno - balanced equation: stroj
výsledek K2Cr2O7 mám jiný.
přes molární hmotnost , kterou násobím 294,19, mi vyjde 8,17g K2Cr2O7
co to vůběc znamená? Děkuji
Offline
#9 07. 03. 2010 20:08
- pavlinkadivisova
- Zelenáč
- Příspěvky: 21
- Reputace: 0
Re: 10% peroxid
↑ jelena:
já netuším, jak mám spočítat teoretický výtěžek....
2K2CrO4 + 2 CH3COOH=2K2Cr2O7 +2 CH3COOK +8 H2O
Offline
#10 07. 03. 2010 20:20
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: 10% peroxid
↑ pavlinkadivisova:
reakce(zkontroluj si to u stroje): 2K2CrO4+2CH3COOH=K2Cr2O7+2CH3COOK+H2O.
Buď v nekterém z předchozích výpočtů máš vypočteno množství K2CrO4, co do reakce vstupuje (já to propočitávám u každé reakce v řetezci), nebo sleduj, jak se mění počet molů (což je náročné a snadno se něco přžehlídne). Vypočetla jsem, že do reakce vstupuje 5,39 g K2Cr04
Z 2 mol K2CrO4 vzníká 1 mol K2Cr2O7
----------------------------------------------
Z 2*M_r K2CrO4 vzníka 1 M_r K2Cr2O7
z 5,39 g K2CrO4 vzníká x g K2Cr2O7
můj výsledek je tedy 4, 086 g. Souhlasí?
------
ve Wolframu se to počítá dobře, protože mohu si přidávát do jednotlivých trojčlenek výsledek předchozí a navazovat (nemusím si zapisovat mezivýpočty).
Offline
#11 07. 03. 2010 20:33
- pavlinkadivisova
- Zelenáč
- Příspěvky: 21
- Reputace: 0
Re: 10% peroxid
↑ jelena:
super, ale nějak nemůžu pochopit, kde vezmu těch 5,39
Offline
#12 07. 03. 2010 20:43
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: 10% peroxid
↑ pavlinkadivisova:
v některé z předchozích reakci bylo, že vzníká 2,863 g Cr(OH)3, teď si projdi jednotlivé reakce (pozor na vyčíslení), až dojdeš k množství 5,39 g K2Cr04.
Já mám zde v tématu jeden mezivýpočet - vznik 4,4196 g K[Cr(OH)4]. Zkus si to překontrolovat.
Offline
#13 08. 03. 2010 10:23 — Editoval jelena (08. 03. 2010 11:42)
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: 10% peroxid
ještě přidám rovnice po opravě, v původním textu bylo nějakých překlepů a nesrovnalosti:
![kopírovat do textarea $\mathrm{Cr(OH)_3 + KOH=K[Cr(OH)_4]}$](/mathtex/50/504ffd4a3cc0302ca89e67d34f09ac33.gif)
![kopírovat do textarea $\mathrm{2K[Cr(OH)_4] + 3H_2O_2 + 2KOH=2K_2CrO_4+ 8H_2O}$](/mathtex/4d/4dca75929fc81a42c87cdf0db92c10f6.gif)
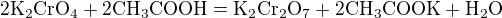
a odkaz na WolframAlpha chemistry.
EDIT: když 2 řádek vynásobim 2 a rovnice sečtu, vychází, že z 1 mol vstupní látky Cr2(SO4)3 vzníká 1 mol produktu K2Cr2O7.
Offline