Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 18. 05. 2011 18:39
- kc_account

- Zelenáč
- Příspěvky: 3
- Reputace: 1
Stechiometricky vzorec
Zdravim,
Pri vypoctu jedne konkretni ulohy vypoctu Stechiometrickeho vzorce jsem zrejme nekde narazil - vysledek se neshoduje s resenim, proto byl byl velice vdecny, kdybyste poukazali mou chybu :).
Zadani:
Pri analyze organicke latky 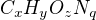 vzniklo z 1g teto latky:
vzniklo z 1g teto latky:
0.013333 mol 
0.03333 mol 
597ml plynneho 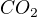 .
.
Pri reakci byl dodavan pouze kyslik. Urcete vzorec teto latky.
Me reseni:
hmotnost C:

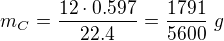
hmotnost N:

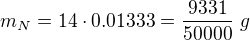
hmotnost H: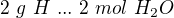
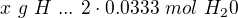

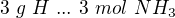
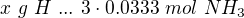
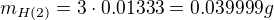

hmotnost O: zbytek do puvodniho mnozstvi 1g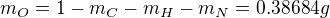
Tady uz nasleduje klasika, kde se podeli hmotnost namereneho vzorku s jeho relativni atomovou hmotnosti, tj.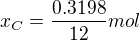
Z vyslednych hodnot se vybere nejmensi hodnota, tou se zbyvajici hodnoty vydeli a vyjdou koeficienty x, y, z a q.
V mem pridade vyslo: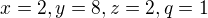
Ovsem zde je ta nesrovnalost s vysledkem, ma vyjit
Velice bych ocenil, kdyby se nekomu z vas podarilo najit chybu, kterou jsem udelal ve vypoctu.
Dekuji :).
Offline
- (téma jako vyřešené označil(a) kc_account)
#2 18. 05. 2011 18:52 — Editoval Pavel Brožek (18. 05. 2011 20:01)
- Pavel Brožek


- Místo: Praha
- Příspěvky: 5694
- Škola: Informatika na MFF UK
- Pozice: Student
- Reputace: 194
Re: Stechiometricky vzorec
↑ kc_account:
Nekontroloval jsem vše, ale podle mě 1g vodíku odpovídá 1 molu vodíku. V 1 molu vody jsou ale 2 moly vodíku. Takže v trojčlence by mělo být
2g H........1 mol vody
Edit: Ať počítám jak počítám, pořád docházím k výsledku 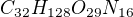 (až na celé násobky). Uvidíme, co řekne Jelena, až přijde. :-)
(až na celé násobky). Uvidíme, co řekne Jelena, až přijde. :-)
Pokud by se u kyslíku „zaokrouhlilo“ 29 na 32 (z důvodu nepřesnosti zadaných čísel), pak bych dostal stejný výsledek jako ty.
Offline
#3 18. 05. 2011 21:00 — Editoval o.neill (18. 05. 2011 21:01) Příspěvek uživatele o.neill byl skryt uživatelem o.neill. Důvod: Mám to blbě
#4 18. 05. 2011 21:31
Re: Stechiometricky vzorec
Ty výpočty hmotností máš nejspíš dobře, v tom konci se nějak ztrácím, třeba nevím co je to xC
Při hledání stechiometrického vzorce se snažíš najít poměr látkových množství jednotlivých prvků. Na vytvoření jedné molekuly NH3 je třeba jeden atom N a tři atomy H. Na vytvoření jedné molekuly H2O je třeba dva atomy H a jeden atom O. Na vytvoření jedné molekuly CO2 je třeba jeden atom C a dva atomy O.
Tedy:
n(C)=n(CO2)=0,597/22,4=0,02665mol
n(H)=2n(H2O)+3n(NH3)=0,10666mol
n(N)=n(NH3)=0,013333mol
S kyslíkem je potíž, že ten tam byl dodáván, je tedy třeba spočítat jeho hmotnost a z ní pak látkové množství
n(O)=m(O)/M(O)=0,38684/16=0,024177mol
Zjišťujeme
n(C):n(H):n(O):n(N)=0,02665:0,10666:0,0241770,01333=32:128:29:16
výsledná látka má tedy stechiometrický vzorec C32H128O29N16
Vyšlo mi to tedy stejně jako kolegovi, doufám, že jsem teď už chybu neudělal.
Offline
#5 18. 05. 2011 22:11
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: Stechiometricky vzorec
Zdravím vás :-)
nám se strojem vychází toto, tedy jako kolegovi ↑ kc_account:, pokud budu zaokrouhlovat. Nebo poměrově - vychází z toho něco lepšího?
Vzali jste ohled, že kyslík se přidával, tedy látka+O2... (kyslík nemusíme urovnávat v základní látce, ale vodík musíme).
Ale já jsem dnes dlouho bojovala o dohled nad klavírem (postupovky se bliží), tak nevím :-) Potom se ještě podívám.
Offline
#6 18. 05. 2011 22:22
Re: Stechiometricky vzorec
↑ jelena:
No však nám to vychází všem stejně, akorát vy dva více zaokrouhlujete.
↑ kc_account:
Řekl bych, že to bude chyba špatně opsaného zadání, protože, využiv Jelenina odkazu, jsem zjistil, že dosadí-li se za množství vzniklé vody 0,013333 mol, tak to vychází přesně 2, 5, 2, 1.
Offline
#7 18. 05. 2011 22:36
- kc_account

- Zelenáč
- Příspěvky: 3
- Reputace: 1
Re: Stechiometricky vzorec
2g H........1 mol vody
Pravda, pri vypoctu se to vykratilo, takze to na vysledek nemelo zadny vliv, dekuji za upozorneni :).
↑ o.neill:
Vskutku, nejspise se nekdo upsal v texu. Diky za snahu, hned mam o jednu 'zahadu' mene ;-).
Dekuji vsem za vase reakce :).
Offline