Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 09. 10. 2011 18:16
- Nanoliquid

- Příspěvky: 64
- Reputace: 0
Výpočty molárních veličin
Dobrý den,
nevím si rady s dvěma příklady. Mohl bych požádat o pomoc ??
1.
Vypočítejte objem 36 % ní HCl o hustotě 1,18 g.cm-3 , který potřebujeme na přípravu 100 cm3 roztoku, jehož molární koncentrace má být 1 mol.dm-3 (Snažil jsem se to řešit pomocí vzorečku pro výpočet molární koncentrace, ale vychází mi to 3,1 . 10-3 dm-3
a druhý příklad :
Vypočítejte, kolik gramů chloridu sodného získáte ze 40 cm3 roztoku hydroxidu sodného o molární koncentraci 1 mol.dm-3
Byl bych moc vděčný za pomoc s tímto příkladem, popřípadě za obrázek s postupem ...Děkuji Moc
Offline
#2 09. 10. 2011 18:50 — Editoval O.o (09. 10. 2011 18:51)
Re: Výpočty molárních veličin
↑ Nanoliquid:
Jak jsi tedy postupoval plus jaký by měl být výsledek, pokud víš, že tvůj není správný?
PS: Nechybí část zadání druhého příkladu?
Offline
#3 09. 10. 2011 19:08 — Editoval Nanoliquid (09. 10. 2011 19:10)
- Nanoliquid

- Příspěvky: 64
- Reputace: 0
Re: Výpočty molárních veličin
Jaký by měl být výsledek právě nevím :(.....
Jinak, 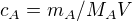 ...do tohoto vzorce jsem za molární hmotnost dal 36,4 g.mol-1 (HCl), za c jsem dal 1 (molární koncentrace) , hustotu 1,18 g.cm-3 jsem si převedl na 1180g.dm-3.....celkový objem ve jmenovateli jsem dal 0,1 dm-3 a hmotnost (v čitateli) jsem si vyjádřil jako hustotu x objem
...do tohoto vzorce jsem za molární hmotnost dal 36,4 g.mol-1 (HCl), za c jsem dal 1 (molární koncentrace) , hustotu 1,18 g.cm-3 jsem si převedl na 1180g.dm-3.....celkový objem ve jmenovateli jsem dal 0,1 dm-3 a hmotnost (v čitateli) jsem si vyjádřil jako hustotu x objem
Ze vzorce jsem si poté vyjádřil objem a počítal.....mám nízké sebevědomí, proto si myslím ,že to mám špatně :)
U druhého příkladu nechybí část zadání.
Offline
#4 09. 10. 2011 19:32
Re: Výpočty molárních veličin
↑ Nanoliquid:
Já se v tom co jsi napsal moc nevyznám, ale jestli jsi to tedy dělal správně, tak ti stále chybí nějaký přepočet, že máš zásobní láhev s 36% HCl, nebo ti to jen uteklo při přepisu sem na forum?
Zkusím to nějak přeložit:
Chceš mít 0,1 dm3 HCl konc. 1 mol/dm3, takže jsi z toho zjistil počet molů (n=CV) a s pomocí molární hmotnosti jsi zjistil tomu odpovídající hmotnost (m(HCl)=Mn), protože máš před sebou láhev w(HCl)=0,36, tak jsi určil hmotnost celého roztoku jako m(roz. 0,36%) = wm(HCl) a přes hustotu jsi získal hledaný objem V(HCl 36%)=m(HCl)/hustota.
Je možné, že jsi to myslel takhle?
U druhého příkladu je, že získáváš NaCl z NaOH, jen mne zajímalo, jeslti jde o neutralizaci.
Offline
#5 09. 10. 2011 19:42
- Nanoliquid

- Příspěvky: 64
- Reputace: 0
Re: Výpočty molárních veličin
A bylo by možné, aby jste poslal(a) postup ??? Těmto dvěma příkladům předcházelo zadání zápisu vzniku NaCl, takže ano, jedná se o neutralizaci HCl + NaOH -> NaCl + H2O .........Sám nevím, jestli jsem to tak myslel, ale bylo mi řečeno, že máme jít přes definici molární koncentrace....O molárních zlomcích nám nic nebylo řečeno
Offline
#6 09. 10. 2011 19:57
Re: Výpočty molárních veličin
↑ Nanoliquid:
Když se na to takhle z dálky koukám, tak bych řekl, že když budeš postupovat podle toho, co jsem napsal "překladu", tak bys se měl dobrat správnému výsledku, zkus to naházet postupně do kalkulačky.
Druhý příklad snad nějak takto:
HCl + NaOH -> NaCl + H2O
m(NaCl) = n(NaCl) * M(NaCl)
n(NaCl) = n(NaOH) = C(NaOH) * V(NaOH)
Offline
#7 09. 10. 2011 20:04
- Nanoliquid

- Příspěvky: 64
- Reputace: 0
Re: Výpočty molárních veličin
Jsem nějaký zmatený z toho ''překladu'' ....Šlo by to prosím napsat tak, jako u posledního příspěvku (př. 2) ??
Offline
#8 09. 10. 2011 20:09 — Editoval O.o (09. 10. 2011 20:39)
Re: Výpočty molárních veličin
↑ Nanoliquid:
Chceš mít 0,1 dm3 HCl konc. 1 mol/dm3, takže jsi z toho zjistil počet molů (n=CV) a s pomocí molární hmotnosti jsi zjistil tomu odpovídající hmotnost (m(HCl)=Mn), protože máš před sebou láhev w(HCl)=0,36, tak jsi určil hmotnost celého roztoku jako m(roz. 0,36%) = wm(HCl) a přes hustotu jsi získal hledaný objem V(HCl 36%)=m(HCl)/hustota.
n(HCl) = C(roztokuHCl) * V(roztoku HCl)
m(HCl) = M(HCl) * n(HCl)
m(roz. 0,36%) = m(HCl) / w(36% HCl)
V(HCl 36%) = m(HCl) / hustota(36% HCl)
(w(36% HCl) = 0,36)
Psal jsem to takto a jen doufám, že jsem to nezvrtal, už mám dnes hlavu z počítání úplně vyždímanou.. .)
Offline
#9 09. 10. 2011 20:24 — Editoval Nanoliquid (09. 10. 2011 20:29)
- Nanoliquid

- Příspěvky: 64
- Reputace: 0
Re: Výpočty molárních veličin
Tak podle postupu mi objem vyšel 1,11 ....jednotka bude cm3 nebo dm3 ?? Jsem už nějaký jetý fakt...:( ....
2. příklad mi vyšel , že získám 2.336 g NaCl ....Mohl bych poprosit o kontrolu správnosti obou výsledků ?? Děkuji mockrát...hlavně za trpělivost
Offline
#10 09. 10. 2011 20:39 — Editoval O.o (09. 10. 2011 20:40)
Re: Výpočty molárních veličin
↑ Nanoliquid:
Drobná chybička se mi tam vloudila, u toho hmotnostního zlomku by nemělo být násobení, ale dělení a ještě obráceně. Nevím, jak proč jsem to sem špatně přepsal. Vyšlo mi to asi 8,59 cm^3.
Druhý příklad mi vyšel stejně jako tobě.
Ještě se sem vrať, aby to někdo zkontroloval, jak vidíš, chyby se mi tam dostanou lehce..
Offline
#11 09. 10. 2011 20:42
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: Výpočty molárních veličin
↑ O.o:
OT: kdo asi bude kontrolovat po jediném oficiálním chemikovi (jsi?) Pozoruješ tuto novou sekci? To je nadělení, musím konstatovat. Zdravím :-)
Nenech se rušit.
Offline
#12 09. 10. 2011 20:44
- Nanoliquid

- Příspěvky: 64
- Reputace: 0
Re: Výpočty molárních veličin
Nerozumím....Hmotnostní zlomek je přece 0,36 ne ?? a u hmotnosti roztoku máte dělení
Offline
#13 09. 10. 2011 20:46
Re: Výpočty molárních veličin
↑ Nanoliquid:
Jak jsem psal příspěvek, že to mám špatně, tak jsem to hend editoval a opravil, takže když si to přepočítáš, jak je to teď, tak to budeš mít určitě správně.
↑ jelena:
Já se jen nepřihalšuji, ale sleduji, všichni odpovídají tak rychle, že když se sem večer dostanu, tak je již vše vyřešené :-). Zase takové nadělení to není, je to jako u nás na škole, prakticky celé tři (až i pět) let jsou to stejné otázky, jak to moc lidí nestihlo pobrat.
Offline
#14 09. 10. 2011 20:50
- Nanoliquid

- Příspěvky: 64
- Reputace: 0
Re: Výpočty molárních veličin
Mohl bych poprosit o napsání řešení ?? Nemůžu se dobrat k vašemu výsledku ....pořád mi vychází 1,11 :(
Offline
#15 09. 10. 2011 20:55
Re: Výpočty molárních veličin
↑ Nanoliquid:
původně jsem tam měl: m(roz. 0,36%) = w(36% HCl) * m(HCl) a tím se dostaneš na těch 1,11.
Opravil jsem to na: m(roz. 0,36%) = m(HCl) / w(36% HCl) (použij tedy tento zápis a uvidíš, že se dopracuješ k správnému výsledku).
Offline