Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 09. 10. 2011 20:00
roztoky
ahoj, začal jsem po letech opět studovat chemii a nevím si rady s pár příklady na roztoky.
1) Jaký objem za normálních podmínek zaujímá množství oxidu uhličitého obsahující
3,011.10^23 atomů kyslíku?
2). Vypočítejte hmotnostní zlomek kyseliny mravenčí v jejím 5,5M roztoku. Hustota roztoku
je 1,056 g.cm^–3
.
3) Jak je třeba mísit 96% kyselinu sírovou s vodou, abychom připravili 0,5 kg 20% roztoku
kyseliny? Hustota 96% kyseliny je 1,835 g.cm^–3
Navštivte portál Matematika pro každého! http://maths.cz
Offline
- (téma jako vyřešené označil(a) jelena)
#2 09. 10. 2011 20:35
Re: roztoky
ad 1) Potřebuješ vědět kolik molů 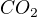 to je. V molekule oxidu uhličitého máš 2 atomy kyslíku, čili počet molů zjistíš jako
to je. V molekule oxidu uhličitého máš 2 atomy kyslíku, čili počet molů zjistíš jako  .
.
A pak buď přes rovnici ideálního plynu vypočítáš objem, nebo si už prostě pamatuješ, že za normálních podmínek má 1 mol plynu objem 
Radim, tedy jsem.
Dobrá rada je drahá, ta moje je zdarma.
Offline
#3 09. 10. 2011 20:40
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: roztoky
↑ Blujacker:
Zdravím,
zkoušel jsi počítat podle návodů v tomto odkazu?
1) CO2 obsahuje uvedený počet atomů kyslíku a poloviční počet atomů uhlíku. Od počtu atomů uhlíku odvodíš počet molů CO2. 1 mol zabírá 22,4 dm^2.
2) c=n/V, w=m(kyseliny)/m(roztoku).
Vezmeš 1 litr roztoku, přes hustotu najdeš jeho m, přes molární koncentraci najdeš n a následně přes M_r najdeš hmotnost rozpuštěné kyseliny,
3) úloha na směsí - hustota kyseliny je zbytečná (jen pokud je třeba dopočíst objem)
Matematicky to určitě zvládneš (a příště, ať nemusím upozorňovat na pravidla spřáteleného fóra :-)
Offline
#4 09. 10. 2011 22:08
Re: roztoky
zdravim, děkuji za rady
1) postupoval jsem podle vašeho návodu, 1 mol zaujímá 22,4 dm^3, 0.25 dm^3 tedy 5.6 dm^3
2)počítal jsem hmotnost přes vzorec m=V*hustota = 1,056 g
pote n=5,5 mol
Mr=46
akorát teď nevím co dosadit za w=1,056/(46+1,056)?
jinak se omlouvám za porušení pravidel, mám spoustu příkladů na vypočítání a většinou nemám tušení ani jak příklad začít řešit..
příště se to nebude už opakovat :)
Navštivte portál Matematika pro každého! http://maths.cz
Offline
#5 09. 10. 2011 22:09
Re: roztoky
zdravim, děkuji za rady
1) postupoval jsem podle vašeho návodu, 1 mol zaujímá 22,4 dm^3, 0.25 dm^3 tedy 5.6 dm^3
2)počítal jsem hmotnost přes vzorec m=V*hustota = 1,056 g
pote n=5,5 mol
Mr=46
akorát teď nevím co dosadit za w=1,056/(46+1,056)?
jinak se omlouvám za porušení pravidel, mám spoustu příkladů na vypočítání a většinou nemám tušení ani jak příklad začít řešit..
příště se to nebude už opakovat :)
Navštivte portál Matematika pro každého! http://maths.cz
Offline
#6 09. 10. 2011 22:44
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: roztoky
počítal jsem hmotnost přes vzorec m=V*hustota = 1,056 g
toto je hmotnost roztoku, ovšem ne OK jednotky: 1 litr nebude vážit 1 g (byť je to kyselina mravenčí).
hmotnost rozpuštěné látky je m(látky) = n*M_r
tedy w=(5,5*46)/1056
Komentář k pravidlům jsem četla (ve všech variantách :-), také věřím. Doporučuji hodně projít odkazy - zrovna toto je velmi podrobně.
Offline
#8 15. 10. 2011 22:32
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: roztoky
↑ pietro:
děkuji :-) nalezeno při úklidu. Já se nechám zapsat větou o označování témat za vyřešená (a o dalším dodržování pravidel).
Jelikož v tématu není žádný vývoj a v úvodním tématu sekce je vyřešených úloh dost, označím za vyřešené.
Offline
