Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 09. 11. 2011 17:47 — Editoval simonaj1 (09. 11. 2011 17:49)
redox rovnice
Ahoj, začnu trošku ze široka
budu mít vyčíslit redox rovnici: 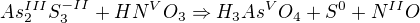
oxidace: 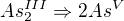 tedy
tedy 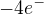 v poměru 1:2
v poměru 1:2
oxidace: 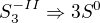 tedy
tedy 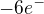 v poměru 1:3
v poměru 1:3
redukce: 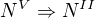 tedy
tedy 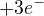 v poměru 1:1
v poměru 1:1
na oxidaci celkem 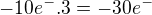 pro arsen a síru koeficient 3
pro arsen a síru koeficient 3
na redukci celkem 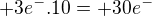 pro dusík koeficient 10
pro dusík koeficient 10
dosadím do rovnice 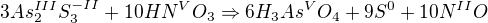 a dopočítám kyslík a vodík na vodu
a dopočítám kyslík a vodík na vodu 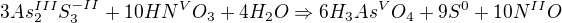
doposud vše jasné, ale budu vyčíslovat rovnici: 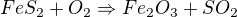 a najednou se úplně ztrácím, je mi jasné, že se redukuje kyslík ale jak to bude s poměry a proč neuvádím ve vyíslení poměry železa? A navíc disulfid železa, jak je to u něj s ox.čísly, nejsem si vůbec jistá... díky
a najednou se úplně ztrácím, je mi jasné, že se redukuje kyslík ale jak to bude s poměry a proč neuvádím ve vyíslení poměry železa? A navíc disulfid železa, jak je to u něj s ox.čísly, nejsem si vůbec jistá... díky
Offline
- (téma jako vyřešené označil(a) jelena)
#2 09. 11. 2011 18:16
Re: redox rovnice
↑ simonaj1: Nemáš v téhle rovnici chybu?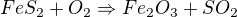
spíš bych to viděl na 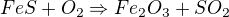
oxiduje 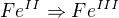
oxiduje 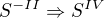
redukuje 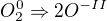
Radim, tedy jsem.
Dobrá rada je drahá, ta moje je zdarma.
Offline
#4 09. 11. 2011 18:40
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: redox rovnice
↑ simonaj1:
Zdravím,
síra v disulfidu je "stejně" jako kyslík v peroxidu H-O-O-H (tedy počítáme celou dvojici kyslíků s oxidačním číslem 2-]. Stejně i v disulfidu síra 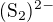 .
.
Usuzuji, že asi neumím počítat "přes poměry" :-) ale snad už si poradíte s kolegou ↑ rleg:, děkuji.
Offline
#6 09. 11. 2011 19:13
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: redox rovnice
Pokud je více prvků zároveň oxiduje (nebo redukuje), tak všechno sečtu za redukující a za oxidující. Pokud je molekula viceatomová (např. kyslik O2), tak napíší jako celek a potom urovnám počet atomu nalevo a napravo:
O2 +4e -> 2O (to je asi "poměry"?)
-----------------------------------------------------
Zde mám:
O2 +4e -> 2O (2-)
----------------------------------
celkem přijato 4e
Fe(2+) -1e -> Fe(3+)
(S_2) (-2) -10e -> 2S (4+)
-------------------------------------
celkem odevzdáno 11e.
Společný násobek 11 a 4 je 44, donásobím 11 řádek kyslíků (nalevo násobím rovnou, napravo jen překontroluji, zda je v součtu 22 kyslíků) a 4 každý řádek Fe, S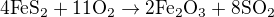
Vyznáš se v tom? Děkuji.
Offline
#7 09. 11. 2011 19:19 — Editoval rleg (09. 11. 2011 19:28)
Re: redox rovnice
↑ jelena: Nechci kalit vodu, ale vychází mi, že disulfid má oxidační číslo -1 (jak podle literatury, tak podle výpočtu)
EDIT: asi už vím, čím to je :o)
↑ simonaj1:
OK, měla jsi tedy zadání dobře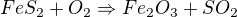
oxiduje 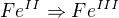
oxiduje 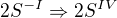
redukuje 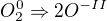
Radim, tedy jsem.
Dobrá rada je drahá, ta moje je zdarma.
Offline
#9 09. 11. 2011 19:26
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: redox rovnice
↑ rleg:
to vychází matematicky :-) ale pokud si představíš, jak je vytvořena vazba, tak každá síra potřebuje dvě pacičky -S-S- , proto píšeme jako skupinu (S2) (2-), ale ne S(1-). Souhlasíš?
↑ simonaj1:
no přesně proto - pokud molekulu nebo skupinu nemůžeme rozdělit, tak musíme psát jako celek, ale železo můžeme "oddělit" s jeho vazbou samostatně.
Offline
#12 09. 11. 2011 19:37
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: redox rovnice
↑ rleg: ano, tak.
↑ simonaj1:
molekulu O=O nerozdělím, protože jeden kyslík nemůže odejít s +2, druhý s -2, molekula byla "nulová".
Skupinu -S-S- nerozdělím (to jsme si ukázali), ale Fe=O rozdělím na Fe(2+), O(2-), stejně tak:
O=Fe-O-Fe=O rozdělím.
Už to, prosím, dodělejte, s kolegou, děkuji a zdar přeji.
Offline

