Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 03. 12. 2011 21:22 — Editoval RabID (04. 12. 2011 17:17)
ph + konc
K 100 ml roztoku ktory obsahovla 0,2 g amoniaku bolo pridano presne stechiometricke mnozstvo kys sirovej o konc 0,5 mol/dm^3. jake je ph v takto vzniklom roztoku siranu amonneho? (pKa NH4 + = 9,245)
postupoval som :
amoniak : kys sirova = 2:1
n(amoniaku) = 0,0118
c(amoniaku) = 0,1176
objem syrovky: 117.6
cez zmiesacku je konc soli 3.244 * 10^-4
2 NH3 + H2SO4 ---> (NH4)2SO4
Ka (NH4+) = 5.688*10^-10
Ka = ( [NH4]^2 * [SO4] ) / [NH4)2SO4]
slaba zasada silna kyselina : pOH= 0.5*(14-pKb-log c(soli)
vobec uz ani nvm co pocitam.
ako mam postupovat dalej nvm si to nejak vyjadrit. Za radu vopred dakujem...
vysledok by mal byt 5,11
Offline
#4 04. 12. 2011 18:16
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: ph + konc
Zdravím,
↑ Yeax:
směšovací rovnici může mít 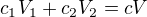 (pro molární koncentrace lze použit - je tak? Děkuji.
(pro molární koncentrace lze použit - je tak? Děkuji.
↑ RabID:
já bych si představovala tak, že sůl vznikla stechiometricky je sůl slabé zásady a silné kyseliny, tedy pH roztoku (kyselé) bude výsledkem hydrolýzy. Ale se samotným výpočtem nejsem si jistá.
Jak dopadla rektifikace? Děkuji :-)
Offline
#6 04. 12. 2011 21:05
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: ph + konc
↑ RabID:
:-) kdyby se mi to podařilo napsat bez nejistých úvah, tak už bych to napsala. Zkusím se na to podívat (dojdu pro knihu). Pokud to někdo vyřeší, budu vděčna :-)
Ještě poznámka - směšovací rovnici jsem napsala pro míchání roztoku o stejné rozpuštěné látce, pro tento příklad neplatí.
Offline
#8 04. 12. 2011 22:33
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: ph + konc
↑ RabID:
asi nebude za co. Početla jsem "Analytickou chemii" - názor na použití hydrolýzy jsem nezměnila :-)
Postupovala bych tak: stechiometricky "vyrobím" (NH4)2SO4 a nechám hydrolyzovat. Tedy nejdřív z reakce vypočtu množství soli a její koncentraci soli (mně vyšla jinak, než Tobě - cca 0,27 mol/l, ale jen tak narychlo).
Potom si představím, že toto množství soli hydrolyzuje a pH= 0.5*(14-pKb-log c(soli)), ovšem pKb pro amoniak je jiné - v mé knize a zde (přepočti, prosím na pKb).
No co si o tom soudíš? Děkuji.
Offline
#9 04. 12. 2011 22:54 — Editoval RabID (04. 12. 2011 23:02)
Re: ph + konc
↑ jelena: no hej vypada to lepsie... prepocet s vysledkom sa sice lisi ale o cca 0,2. No ale toto vypada aspon trochu k svetu :)
ja som to tiez potom zobral z takehoto konca. len ma stve ze mne vychadza 0,027 mol/l ale taktiez sa to lisi o
cca 0,2.
pKb vyslo 4,755
Offline
#10 04. 12. 2011 23:07
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: ph + konc
↑ RabID:
Mně tak úplně nesedí, že sčítáme objemy reagujících roztoků (bez přepočtu na hmotnost), ale jinak se mi takový postup zdá použitelný a zdůvodnitelný. Snad to ještě probereš s kolegy ve škole.
Offline
#13 11. 12. 2011 09:39
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: ph + konc
↑ RabID:
Také pozdrav :-) za ten týden už jsi mohl dojit (i s kolektivem kolegů) na konzultaci, že ano? Prošla jsem to celé: FMEA u ranní kávy - zdroje chyb mohou být:
a) v samotném systému výpočtu (bereme, že nejdřív vznikne sůl a potom řešíme její hydrolýzu) - mně se to zdá v pořádku, můžeme ještě uvažovat 2. stupeň hydrolýzy, ale nechce se nám.
Zkoušela jsem počítat i přes rovnovážnou konstantu (cca stejný výsledek) - viz odkaz str. cca 130 (českou/slovenskou verzi se mi nechce hledat). V odkazech máme sbírku řešených úloh - už se mi nechce hledat, zda to tam není.
b) tabulkové hodnoty pKb - jsme opravili,
c) výpočtové chyby závažné - našla jsem jen, že objem syrovky: 117.6 má být 11,76 - souhlasí? (a asi sírovky :-).
d) překlepy ve výpočtu - nenašla jsem (počítala jsem s opravenou hodnotou objemu)
e) zanedbání hustoty a počítání součtu objemů - našla jsem tabulkové hodnoty hustot, vliv je zanedbatelný,
----------------------------------
vychází mi pH=5,27 k lepšímu výsledku jsem se nedostala. Ale došla jsem, jak ušetřit čas při plnění úkolu strany a vlády, půjdu požádat o rozhodnutí (strana a vláda neříkala "hledat pH", ale něco zcela jiného :-)
Offline
#15 11. 12. 2011 13:29
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: ph + konc
↑ RabID:
Já také :-) zkus ještě projít řešené úlohy "okolo č. 110", děkuji.
-------------------
я Тебе конечно верю, разве могут быть сомненья :-)
Offline
