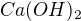Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#3 08. 12. 2011 20:00
Re: Hydroxid
No,reaktivita kovového vápníku a barya je prakticky shodná.
S obojím jsem pracoval,mohu tedy potvrdit.
Nás ale bude zajímat srovnání rozpustností(tedy disociačních konstant) hydroxidů:
hořečnatý
vápenatý
barnatý
no a tady to baryum vede.
Ni moc, ni bohatství, jen vědění žezla trvají!
Offline
#4 08. 12. 2011 23:07
Re: Hydroxid
Ja bych doplnil , že podle mě je silnější hydroxid barnatý a to z důvodu nižší polarizační síly kationtu 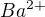 . Polarizační síla je schopnost kationtu deformovat elektronový obal aniontu , roste se zvetsujicim se nabojem kationtu a se zmensujicim polomerem kationtu . Protože
. Polarizační síla je schopnost kationtu deformovat elektronový obal aniontu , roste se zvetsujicim se nabojem kationtu a se zmensujicim polomerem kationtu . Protože 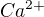 je menší kationt nez
je menší kationt nez  více deformuje elektronový obal
více deformuje elektronový obal 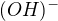 a čím větší je deformace tím je vazba mezi kationtem a aniontem kovalentnejší . A čim menší je deformace
a čím větší je deformace tím je vazba mezi kationtem a aniontem kovalentnejší . A čim menší je deformace 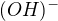 tak tim je vazba mezi kationtem a aniontem iontovější . A iontovější látky jsou lépe rozpustné ve vodě .
tak tim je vazba mezi kationtem a aniontem iontovější . A iontovější látky jsou lépe rozpustné ve vodě .
Poznamka :
U aniontů mluvíme o polarizovatelnosti a trend je tam presne opacny , čím je aniont zápornější a větší tím má větší polarizovaletnost . S rostoucí polarizovatelnosti aniontu roste deformace kationtu a tím se opět vazba stává kovaletnější .
Snad sem pomohl .
Offline