Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 13. 12. 2011 11:11
Vznik 50l chloru
Dobrý den, potřebovala bych poradit s příkladem, který mi nevychází podle výsledků. Moc vám děkuji
Jaké množství MnO2 a kolik ml 36% HCl o hustotě 1,179 g/cm3 musí zreagovat, aby vzniklo 50l chloru?
Napsala jsem si rovnici: MnO2 + HCl 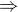 MnCl2 + Cl2+H2
MnCl2 + Cl2+H2
Pak jsem si vypočítala hmotnost 100% HCl: m=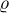 * V = 1,179*50= 58,95 g
* V = 1,179*50= 58,95 g
Hmotnost 36% mi vyšla 163,75 g
Množství MnO2: (163,75/36,5)*87=390 a mělo by vyjít 194g. Děkuju za radu
Offline
#2 13. 12. 2011 11:48 — Editoval rleg (13. 12. 2011 11:53)
Re: Vznik 50l chloru
↑ Týna:
Ahoj
začal bych tím, že bych tu rovnici napsal správně a vyčíslil ji
předpokládám, že bude vypadat nějak takto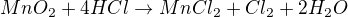
čili vidím, že na 1 mol plynného chlóru mi do reakce musí vejít 4 moly chlorovodíku
Budu předpokládat standardní podmínky a z nich vypočtu kolik molů chlóru má vzniknout 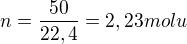
do reakce mi tedy musí vejít 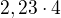 molů HCl, tj. 8,92 molů
molů HCl, tj. 8,92 molů
Potřebnou hmotnost HCl dostanu jako součin molárního množství a hmotnosti 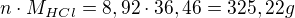
Potřebný objem HCl dostanu jako 
A co se týče hmotnosti 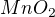 tak zase platí, že na 1 mol vzniklého chlóru připadá 1 mol
tak zase platí, že na 1 mol vzniklého chlóru připadá 1 mol 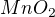 , které musí vstoupit do reakce, čili
, které musí vstoupit do reakce, čili 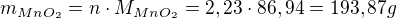
Radim, tedy jsem.
Dobrá rada je drahá, ta moje je zdarma.
Offline
