Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 14. 04. 2012 10:18 — Editoval terezkaaaaa5 (14. 04. 2012 10:21)
- terezkaaaaa5

- Příspěvky: 1221
- Reputace: 2
Práce vykonaná plynem
Dobrý den, poradíte mi prosím s tímto příkladem? Díky moc.
Vodík má hmotnost 5kg a teplotu 0°C. O kolik se musela zvýšit jeho teplota, aby při izobarickém ději vykonal práci 37,4 kJ?
Vím, že tam bude hrát roli vzoreček 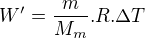 , ale nějak si s tím nevím rady.
, ale nějak si s tím nevím rady.
Offline
- (téma jako vyřešené označil(a) terezkaaaaa5)
#3 14. 04. 2012 10:49 — Editoval Nautileus (14. 04. 2012 10:50)
Re: Práce vykonaná plynem
↑ terezkaaaaa5:
Ahoj,
V prvé řadě ti opravím ten vzoreček, který latex píše jako fail, očividně mu ta čárka nesvědčí: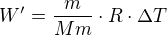
A teď k tvému příkladu, již se to tu řešilo Zde
Dovolím si citovat konečný příspěvek z toho vlákna od Pavla Brožka, který by ti měl dostatečně pomoci:
Zjistit látkové množství z hmotnosti snad zvládneš.
║▌│█│║▌║││█C║h▌a│o║S▌║█║▌│█│║▌║
S∞=0100101001001010010100100101001001…
... 1 0 1 1 0 1 0 1 1 0 1 1 0 1 0 1 1 0 1 ...
█║▌│█│║▌║││█║▌│║▌║█║▌│█│║▌║││█║▌│║
Offline
#4 14. 04. 2012 10:56 — Editoval terezkaaaaa5 (14. 04. 2012 11:04)
- terezkaaaaa5

- Příspěvky: 1221
- Reputace: 2
Re: Práce vykonaná plynem
↑ Nautileus:
Díky. Ale vzoreček, který jsem napsala je podle mého shodný s tím citovaným. Ale stejně si s tím nevím moc rady.
Respektive, si nevím rady právě s tou molární hmotností. Vzorec by měl být 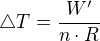
Offline
#5 14. 04. 2012 11:18 — Editoval Nautileus (14. 04. 2012 11:27)
Re: Práce vykonaná plynem
↑ terezkaaaaa5:
Dobrá tedy, myslel jsem, že ti to rozepsání pomůže.
Takže polopatě:
m = 5 kg
t1 = 0 °C -> T1 = 273 K
deltaT = ?
p = konst.
W´ = 37,4 kJ = 37,4 . 10^3 J
R = 8,31 J . K^-1. mol^-1
MmH = 2 . 10^-3 kg . mol^-1
----------------------------------------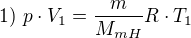
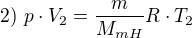
Odečteš od rovnice 2 rovnici 1 a vytkneš: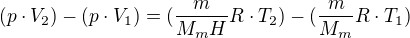
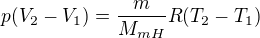
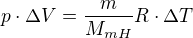
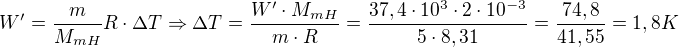
║▌│█│║▌║││█C║h▌a│o║S▌║█║▌│█│║▌║
S∞=0100101001001010010100100101001001…
... 1 0 1 1 0 1 0 1 1 0 1 1 0 1 0 1 1 0 1 ...
█║▌│█│║▌║││█║▌│║▌║█║▌│█│║▌║││█║▌│║
Offline
#6 14. 04. 2012 11:25
- terezkaaaaa5

- Příspěvky: 1221
- Reputace: 2
Re: Práce vykonaná plynem
↑ Nautileus:
Díky. Jen se chci zeptat, jak přijdu na MmH?
Offline
#7 14. 04. 2012 13:15
Re: Práce vykonaná plynem
↑ terezkaaaaa5:
MmH je molární hmotnost vodíku, pokud není zadaná, tak molární hmotnost odpovídá relativní molekulové hmotnosti: 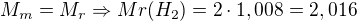
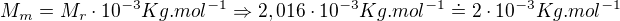
kde 1,008 je atomová hmotnost vodíku a najdeš ji u prvku vodíku v PT.
║▌│█│║▌║││█C║h▌a│o║S▌║█║▌│█│║▌║
S∞=0100101001001010010100100101001001…
... 1 0 1 1 0 1 0 1 1 0 1 1 0 1 0 1 1 0 1 ...
█║▌│█│║▌║││█║▌│║▌║█║▌│█│║▌║││█║▌│║
Offline