Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 21. 05. 2012 17:47
Výpočet pH
Ve 2,4 l roztoku bylo rozpuštěno 0,4 g NaOH a 0,49 g kyseliny sírové, jaké bude pH roztoku?
Vím že nejdříve musím vypočítat koncentraci látky která bude ve výsledném roztoku v přebytku a pak pH odvíjí od ní. Jen je tady problém s tvou dvojsytnou sírovou. Nevím jak to mam dosadit aby mi to vyšlo. Už sem i vyčislovala rovnici a pořad mi to nevychazi.
Offline
#2 21. 05. 2012 19:22
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: Výpočet pH
Opět pozdrav,
co tedy vyšlo v přebytku? Potom ještě proběhla reakce a pouze zbytek zajišťuje výsledné pH. Piš, prosím, celé výpočty.
Pokud kyselina, tak vzorec pro pH musí zohledňovat dvojsytnost. 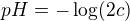
Ty se chystáš na medicinu? Děkuji.
Offline
#3 21. 05. 2012 20:06
Re: Výpočet pH
↑ jelena:
2 NaOH + H2SO4  Na2SO4 + H2O
Na2SO4 + H2O
N NaOH = 0,4/40 = 0,01 mol x 2 = 0,02 mol
n h2so4 = 0,49 / 98 = 5 x 10 na -3
n = n NaOH - n h2so4 = 0,015
c = n / V = 0,015 / 2,4 = 6,25 x 10 na -3 mol / l
pH = -log c = po dosazení by mělo vyjít 7 a mě vychazi 2,2
Offline
#4 21. 05. 2012 21:55
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: Výpočet pH
Zohlednila jsi, že 1 mol H2SO4 reaguje s 2 mol NaOH?
N NaOH = 0,4/40 = 0,01 mol x 2 = 0,02 mol - to jsi domyslela, to nemá být.
k dispozici máme 0,01 mol NaOH a 0,005 mol H2SO4 (0,01:0,005=2:1) - to je realita.
Podle reakce také 1 mol H2SO4 reaguje s 2 mol NaOH, tedy u nás je situace přesně rovnovážná a nic není v přebytku, proběhne reakce neutralizace, proto pH=7.
V pořádku?
Offline
