Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 21. 09. 2012 13:50 — Editoval Vladislav97 (21. 09. 2012 13:53)
- Vladislav97

- Místo: Praha
- Příspěvky: 421
- Škola: Gymnázium
- Pozice: Student (Druhák)
- Reputace: 13
Síran zinečnatý (ZnSO4)
Zdravím, mám zase problém ze zapsání jedné soli. Viz nahoře. Kyselina od toho je 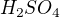 Tim pádem:
Tim pádem: no, a pak by vzniklo
no, a pak by vzniklo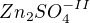 . Ale ve výsledku není ten dolní index u zinku. Proč? Protože má zinek -II? Předem moc děkuji za vysvětlení!
. Ale ve výsledku není ten dolní index u zinku. Proč? Protože má zinek -II? Předem moc děkuji za vysvětlení!
Offline
#2 21. 09. 2012 15:41
Re: Síran zinečnatý (ZnSO4)
Molekula má být neutrální částice. Správně jsi určil, že síranový aniont má náboj 2- (římskými číslicemi se píší pouze oxidační čísla jednotlivých prvků, náboje píšeme arabskými). Máme-li vytvořit neutrální sůl, pak potřebujeme molekulu vytvořit tak, aby na jeden síranový aniont připadal náboj 2+, aby se náboje vyrušily. Kdybychom měli síran sodný, pak bychom z názvu vyvodili, že sodík má v této sloučenině oxidační číslo I, sodný kationt tedy bude mít náboj 1+, potřebujeme tedy dva sodné kationty na jeden síranový anion, aby se náboje vyrušily, síran sodný tedy bude Na₂SO₄. V síranu zinečnatém je zinek v oxidačním čísle II, zinečnatý kationt tedy má náboj 2+ a s nábojem síranového aniontu se tento náboj vyruší a máme rovnou neutrální molekulu, vzorec síranu zinečnatého je tedy ZnSO₄. Kdybychom měli síran hlinitý, kde je hliník v ox. č. III, má tedy náboj 3+, jsou na neutrální molekulu třeba dva hlinité kationty a tři síranové anionty, jinak to nejde, vzorec by tedy byl Al₂(SO₄)₃.
Offline
#3 21. 09. 2012 18:28 — Editoval Vladislav97 (21. 09. 2012 18:29)
- Vladislav97

- Místo: Praha
- Příspěvky: 421
- Škola: Gymnázium
- Pozice: Student (Druhák)
- Reputace: 13
Re: Síran zinečnatý (ZnSO4)
↑ o.neill: Já moc tedy nechápu, proč má tedy zinek ox. +II. To je tak daný? Mohl bych poprosit, jak se ten vzorec z názvu postupně zapisuje? Abych sledoval postup?
(NEBO I OSTATNÍ)
Offline
#4 21. 09. 2012 18:43
- Vladislav97

- Místo: Praha
- Příspěvky: 421
- Škola: Gymnázium
- Pozice: Student (Druhák)
- Reputace: 13
Re: Síran zinečnatý (ZnSO4)
Jo to hlavně nechápu...já jsem pak přece použil křížový pravidlo. U všeho mi to vždy jde, ale tady nějak prostě ne.
Offline
#5 21. 09. 2012 20:12
Re: Síran zinečnatý (ZnSO4)
↑ Vladislav97:
Ahoj
říká ti ještě něco -ný,-natý,-itý,-ičitý,-ičný/-ečný,-ový,-istý,-ičelý? :o) Přesně tohle v názvu ti říká jaké oxidační číslo ten zinek bude mít.
Radim, tedy jsem.
Dobrá rada je drahá, ta moje je zdarma.
Offline
#6 21. 09. 2012 20:20
- Vladislav97

- Místo: Praha
- Příspěvky: 421
- Škola: Gymnázium
- Pozice: Student (Druhák)
- Reputace: 13
Re: Síran zinečnatý (ZnSO4)
↑ rleg: Takže: 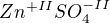 ->
->
Offline
#7 21. 09. 2012 23:17
Re: Síran zinečnatý (ZnSO4)
↑ Vladislav97:
ju, přesně tak
Radim, tedy jsem.
Dobrá rada je drahá, ta moje je zdarma.
Offline