Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 26. 11. 2012 16:00
Titrační křivka
Zdravím,
nevím, jak vypočítat tento příklad.
K titraci odpipetováno 50 ml roztoku NH3 o c=0,05mol/l a titrováno odměrným roztokem 0,05M H2SO4.
Nakresli titrační křivku a vypočti pH.
V(ml) 0 10 20 24 24,9 25 25,1 26 30
pH ?
Nemohl by mi prosím někdo poradit, jak vůbec začít s tímto příkladem.
Napsala jsem si rovnici:
H2SO4 + 2 NH3 >> ( NH4)2SO4
ale nevím, jak pokračovat.
Děkuji
Offline
#2 26. 11. 2012 20:39
Re: Titrační křivka
Zdravím. Následující postup pouze, pokud nemáte pracovat s disociační konstantou:
Vodný roztok NH3 je v podstatě jakoby molekula NH4OH. Tato disociuje na NH4+ a OH-. Pokud je disociace úplná, poté se koncentrace OH- iontů rovná koncentraci čpavku. 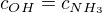 z toho
z toho 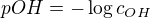 a
a 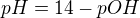 Ovšem při titraci se bude snižovat koncentrace OH iontů tím, jak se bude měnit NH4OH na (NH4)2SO4. A s tím je nutno počítat.
Ovšem při titraci se bude snižovat koncentrace OH iontů tím, jak se bude měnit NH4OH na (NH4)2SO4. A s tím je nutno počítat.
Doučím M, Ch v okolí Pardubic
Press any key to continue. Alt + F4?
Offline
#5 27. 11. 2012 12:15
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: Titrační křivka
Zdravím,
zde jsou 2 úlohy - do okamžiku bodu ekvivalence převažuje v roztoku NH4OH a ten dává výsledné pH roztoku. pH (pOH) se počítá jako pH (pOH) slabé zásady, tedy s použitím K NH3 z tabulek.
Bod ekvivalence se vypočte tak, že látkové množství přidaného H2SO4 je přesně polovina látkového množství NH3 v roztoku (tedy přesně podle reakce, jak jsi sestavila). Před bodem ekvivalence také počítáš spotřebu NH3 a kyseliny dle reakce, ovšem výpočet se vede dle kyseliny, jelikož je v nedostatku. NH3 převažující se použije pro výpočet pH (pOH).
Po bodu ekvivalence převažuje kyselina, přebytečná bude dávat pH a je to kyselina silná. Tedy jiný vzorec pH pro silné kyseliny.
Zorientuješ se tak? Děkuji.
Offline

