Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
Stránky: 1
- Hlavní strana
- » Chemie
- » Strukturní vzorce (domácí procvičování No. 1/3) (TOTO TÉMA JE VYŘEŠENÉ)
#1 17. 02. 2013 18:39 — Editoval Vladislav97 (18. 02. 2013 09:18)
- Vladislav97

- Místo: Praha
- Příspěvky: 421
- Škola: Gymnázium
- Pozice: Student (Druhák)
- Reputace: 13
Strukturní vzorce (domácí procvičování No. 1/3)
1 část ze 3
Obrázky jsou nyní funkční
Dobrý den,
ve škole jsme začali nové téma, které se snažím pochopit. Profesorka nám dala pracovní papír, který si můžeme dobrovolně vypracovat, a tedy procvičit látku, kterou budem opět psát za týden. Papír obsahuje 3 sady vzorců, kde z každé sady udělám jedno téma. Já bych vás chtěl poprosit, pokud byste mi nezkontrolovali moje postupy a řešení, poradili mi, co je správně a co není, a také doplnily moje chybějicí údaje. Předem vám moc děkuji za pomoc.
Zadání:
1. sada vzorců:
Pomocný papír, který nám profesorka dala:
Moje řešení:
Offline
- (téma jako vyřešené označil(a) Vladislav97)
#2 18. 02. 2013 09:19
- Vladislav97

- Místo: Praha
- Příspěvky: 421
- Škola: Gymnázium
- Pozice: Student (Druhák)
- Reputace: 13
Re: Strukturní vzorce (domácí procvičování No. 1/3)
↑ Vladislav97: Obrázky jsou nyní funkční.
Offline
#3 18. 02. 2013 13:12
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: Strukturní vzorce (domácí procvičování No. 1/3)
Zdravím,
já bych řekla, že obrázky byly funkční včera :-) Ale je možné, že aktuálně z bezpečnostních důvodů mám nepovoleno prohlížet - zeptám se.
Včera jsem zkoušela projít, ale mám moc vlastního psání, tedy teď je to pro mne moc velký soubor na pořádné procházení - snad kolegové (nebo si to zkonzultuj s paní učitelkou ještě před testem), případně jen něco zkontroluji. Pokud si vybavuji, největší problém byl s hybridizaci - ta by měla být uvažována pouze v případě, že pro vznik vazeb elektrony přechází ze základního do excitovaného stavu (pokud to není a je dost nespárovaných elektronu, potom neuvažujeme hybridizaci - je tak?).
V odkazech jsou animace, jinak takových animací je celkem dost (asi AJ). Jinak paní učitelka to bere pěkně pořádně - vy se specializujete na přírodní vědy, nebo je to váš standard (psal jsi, že hodně dobrá škola)? Děkuji.
Offline
#4 18. 02. 2013 13:31 — Editoval Vladislav97 (18. 02. 2013 13:35)
- Vladislav97

- Místo: Praha
- Příspěvky: 421
- Škola: Gymnázium
- Pozice: Student (Druhák)
- Reputace: 13
Re: Strukturní vzorce (domácí procvičování No. 1/3)
↑ jelena:
Také zdravím,
no, právě že vůbec toto gymnázium není zaměřený na žádný konkrétní obor - je všeobecné. Ale pořád mám pocit, jako kdybych se tam učil jen a jen chemii. Co se týče toho, abychom tento papír projít před testem, tak tuto nabídku profesorka s pološirokým úsměvem ignoruje. My totiž každý týden píšem alespon jeden test, což je poměrně trochu dost.
Cose týče obrázku, tak se každou chvíli vypařej. Já je tam zkusim dat jiným způsobem, at jsou tam už nastálo :-). Pokud by se našel nějak čas to zkontrolovat, budu vděčný. Ono to tak úplně nespěchá, jelikož mám zatim týden prázdnin :-).
Do pěti minut by už měli obrázky jít.
Já ted vůbec nemůžu ani editovat svoje téma :-(
Offline
#5 18. 02. 2013 13:39 — Editoval Vladislav97 (18. 02. 2013 13:40)
- Vladislav97

- Místo: Praha
- Příspěvky: 421
- Škola: Gymnázium
- Pozice: Student (Druhák)
- Reputace: 13
Re: Strukturní vzorce (domácí procvičování No. 1/3)
Teď by to už muselo jít. (Aktualizováno)
Zadání:
1. sada vzorců:
Pomocný papír, který nám profesorka dala:
Moje řešení:
Offline
#6 18. 02. 2013 20:18
- Vladislav97

- Místo: Praha
- Příspěvky: 421
- Škola: Gymnázium
- Pozice: Student (Druhák)
- Reputace: 13
Re: Strukturní vzorce (domácí procvičování No. 1/3)
↑ jelena: No, vidím, že asi bude lepší, abych se zítra zeptal na konkrétní věci. :)
Offline
#7 18. 02. 2013 20:38
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: Strukturní vzorce (domácí procvičování No. 1/3)
↑ Vladislav97:
děkuji za doplnění, obrázky funguji. Pokud to tedy nijak nehoří, tak bych se podívala ve čtvrtek za denního světla. Do té doby snad i někdo z kolegů něco zkontroluje.
Zatím bych řekla, že největší problém s excitovaným stavem a určením hybridizace (jelikož se od toho odvozuje). Jelikož strukturní vzorce máš (podrobně jsem nekontrolovala), začni vždy kontrolou, zda základní stav elektronové konfigurace umožní zabezpečit požadovaný počet vazeb. Podmínkou však je, aby byla dostupná volna orbital s blízkou energetickou úrovni. Např. jak jste si vysvětlovali vazby s dusíkem? To jen na úvod. Děkuji a sněhové prázdniny přeji.
Offline
#8 18. 02. 2013 20:52
- Vladislav97

- Místo: Praha
- Příspěvky: 421
- Škola: Gymnázium
- Pozice: Student (Druhák)
- Reputace: 13
Re: Strukturní vzorce (domácí procvičování No. 1/3)
↑ jelena: Tak jo, děkuji moc. Vazby s dusíkem jsme si vůbec nevysvětlovali, ale mám dojem, že jsem u HCN zapomněl dodat u N jeden volný elektronový pár (aby tam bylo celkem 5 vazeb).
Ještě takový menší objasnění, proč jsem u některých vzorců napsal, že nevím, jak udělat excitovaný stav.
Nejdříve si udělám si základní stav centrálního atomu. Pak hledám takový excitovaný stav, aby vždy pouze jeden elektron ve "čtverečku" představoval jednu vazbu.
Např.  http://postimage.org/image/x4zzjzqd1/ . Mám tam
http://postimage.org/image/x4zzjzqd1/ . Mám tam  , což je dohromady 4 vazby. A také proto jsem udělal excitovaný stav tak, aby tam byly pouze 4 "čtverečky" pouze s jedním elektronem, kde orbital s jako vazbu nepočítám. A pak pouze jeden elektron škrtnu, jelikož tam mám jednu vazbu
, což je dohromady 4 vazby. A také proto jsem udělal excitovaný stav tak, aby tam byly pouze 4 "čtverečky" pouze s jedním elektronem, kde orbital s jako vazbu nepočítám. A pak pouze jeden elektron škrtnu, jelikož tam mám jednu vazbu 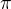 . Poté napíšu, kde mi tento postup nevycházel.
. Poté napíšu, kde mi tento postup nevycházel.
P.S. Děkuji za přání :-)
Offline
#9 19. 02. 2013 00:33
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: Strukturní vzorce (domácí procvičování No. 1/3)
↑ Vladislav97:
no to je pravě taková potíž - dusík nemá možnost se dostávat do excitovaného stavu (alespoň si to myslím), protože není energeticky blízká orbital, kam by se dalo "přeskočit". Tedy v molekulách, kde je dusík centrální atom postup vzniku vazby je jiný, než excitace.
jelikož se mi nechce hledat, tak umístím alespoň náhled na obrázky, jak vzniká vazba - a proto se ptám - jak vysvětlovala paní učitelka (nebo alespoň podle které knihy berete). Abych řekla pravdu, tak jsem ještě neprocházela VŠCHT "Anorganiku nekovu", tam by to mohlo být také. Nechám to ne Tebe nebo až na čtvrtek :-)
U síry ano - tam už 3d je blízko, proto skok je možný (ovšem potom v zápis se má objevit, že v tvorbě vazby se účastní s, p, d (tedy hybridizace p3d pro S(4+) a sp3d2 pro S(6+) - počítám dobře?)
Offline
#10 19. 02. 2013 18:32
- Vladislav97

- Místo: Praha
- Příspěvky: 421
- Škola: Gymnázium
- Pozice: Student (Druhák)
- Reputace: 13
Re: Strukturní vzorce (domácí procvičování No. 1/3)
↑ jelena: Řekl bych, že to necháme asi až na ten čtvrtek. Ve škole chemii vůbec podle žádné knížky nebereme.
S tou vazností u síry bych řekl, že je vše v pořádku.
P.S. kouknul jsem se na ten odkaz a do čtvrtka se to ještě pokusim přečíst (umim rusky). :-)
Offline
#11 21. 02. 2013 12:11
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: Strukturní vzorce (domácí procvičování No. 1/3)
Zdravím,
kontroluji, jak jsem slíbila (počasí je na kontrolu pohádkové - je zataženo a sněží :-).
H2SO3, H2SO4, H2S2O7 - jen chybí hybridizace (hybridizaci odvozujeme od excitovaného stavu)
H2S - excitaci není (protože není nutná), také není hybridizace, struktura molekuly lineární lomena (obdobné zdůvodnění jako u molekuly H2O, ovšem bez vodíkových vazeb).
HClO - hybridizaci, ani excitaci neuvažujeme, tvar molekuly, z důvodu polarity nemůže být lineární.
HClO2, HClO3 - hybridizaci odvozujeme od excitovaného stavu, pravděpodobnosti strukturu - buď podle počtu elektronových párů, co tvoří hlavní vazby a tedy podle prvního sloupce tabulky (nebo škrtneme d a dostaneme tvar podle zbývající konfigurace centrálního atomu).
HClO4 - pro vytvoření všech vazeb je třeba ještě excitovat 1 elektron z 3s2.
HBO2 - v excitovaném stavu 1s a 2p, proto hybridizace je sp2
H3BO3 - trihydrogenboritá, nebo předchozí monoboritá :-)
HPO3 - pokud máš dvojnou vazbu, jedna ve dvojné je "sigma", druhá je "pi" - to chybí, excitovaný tvar je třeba, tedy bude i hybridizace.
H3PO4 - trihydrogenfosforečná nebo předchozí ...:-) Poznámka - co do struktury centrálního atomu HPO3 a H3PO4 jsou stejné, jen je u H3PO4 menší počet dvojných vazeb, protože kyslík se zabaví jinak.
HNO2 - není třeba excitaci, tedy není ani hybridizace
HNO3 - jsme diskutovali, podle mne nemůže vytvářet excitovaný stav
HCN - excitace centrálního atomu C je klasika ve všech učebnicích :-) Zkus ještě jednou. Opět - pokud máš trojnou vazbu, jedna z "trojky" je vazba "sigma", zbytek jsou "pi"
projdeš to ještě jednou (netvrdím, že jsem něco nevynechala)? Děkuji.
Offline
#12 21. 02. 2013 17:36
- Vladislav97

- Místo: Praha
- Příspěvky: 421
- Škola: Gymnázium
- Pozice: Student (Druhák)
- Reputace: 13
Re: Strukturní vzorce (domácí procvičování No. 1/3)
↑ jelena:
Zdravím,
děkujii moc za opravu :-).
Jdu se tedy ptát...
H2SO3, H2SO4, H2S2O7 - Tu hybridizace mám špatně?
H2S - Rozumím
HClO - Takže tvar neurčuji?
HClO2, HClO3 -
takže HClO2 bude mít hybridizaci sp2 a tim pádem tvar molekuly bude lineární (+ dva volné elektronové páry)?
u HClO3 nemůžu najít chybu.
HClO4 - Nedokážu vytvořit excitovaný stav. Vždy, když vytvářím excitovaný stav, koukám se kolik má celkem vazeb. Zde je to  což je dohromady 4. V excitovaným stavu se vždy snažim docílit toho, abych měl dohromady ve všech "čtverečcích" pouze 4 samostatné elektrony.
což je dohromady 4. V excitovaným stavu se vždy snažim docílit toho, abych měl dohromady ve všech "čtverečcích" pouze 4 samostatné elektrony.
Když zkusim 1. excitovaný stav, tak budu mít:
To ale mám pak 3 elektrony, ale já potřebuji 4.
Když zkusim 2. excitovaný stav, tak budu mít:
Zde más zase ale 5 elektronu, a to mi na 4 vazby nevychází.
HBO2 - Moc nechápu. Já topiž vždy zapíšu počet osamocených elektronů, které mi tam zůstanou. Po škrtnutí mi tam zůstanou jenom dva osamocené elektrony, tak moc nechápu proč sp[color=gŕed]2[/color]
H3BO3 - Rozumím :-)
HPO3 - Ano, už vidim tu chybičku :-). Tedy hybridizace je sp2?
H3PO4 Jinak je to vše správně?
HNO2 Takže i přesto, že tam je pí vazba, škrtat elektrno nemusím? Určuje se tedy pak i tvar molekuly?
HNO3 - Když tak se ještě zeptam profesorky na to a uvidím, co mi na to řekne :-)
HCN - Určitě vim, že jsou tam
 a pak je tam tedy i jedna
a pak je tam tedy i jedna 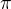
? A ještě to trojná vazba, ta se nějak zapisuje?
Vidím to tak, že jsem už asi další sady tahat nebudu, asi jen pár vzorců, se kterými budu mít problém. :-)
Offline
#13 22. 02. 2013 00:36
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: Strukturní vzorce (domácí procvičování No. 1/3)
↑ Vladislav97:
Také pozdrav a děkuji,
já se pokusím podívat a odpovědět snad v sobotu :-) Mám z tohoto tématu podivný pocit - nevím, jakou formou paní učitelka vám celý problém přiblížila - už jsem se ptala - jak vysvětlovala, co máte v sešitu - nejde nascanovat? (kniha není, jak jsem pochopila).
Podrobnější vysvětlování bez kreslení obrázku si nějak neumím představit, bohužel.
Zkus ještě si z ulozto stáhnout učebnici Klikorka, Hájek, Votinský - Obecná a anorganická chemie.pdf Jsou to celkem drobnosti, v čem se neshodujeme, ale mám dojem, že pořádné vysvětlení z knihy (hybridizace) bude mít větší užitek, než mé bla-bla :-)
Offline
#14 23. 02. 2013 21:37
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: Strukturní vzorce (domácí procvičování No. 1/3)
Slíbila jsem, že dopíší v sobotu, tak ještě snad splním.
Vidím potíž v tom, že máš určitou techniku a označení, které mi není zcela jasné. A proto nechci měnit systém paní učitelky, pokud nějaký nasadila (mám dojem, že Klikorkou je dost ovlivněna, tedy měli bychom být ve shodě :-) Snad se zeptej paní učitelky, zda můžete studovat podle Klikorky - je to taková klasika, dá se vypůjčit v knihovně.
Popíši to tak, jak já bych postupovala - případně to s paní učitelkou ještě konzultuj.
a) hybridizaci beru vždy až po excitaci - důvod je ten, že až po "vlezení" na "cizí pozemek" elektron je donucen se přetvařovat, že jeho orbital vypadá jinak. Aby se nepoznalo, který elektron ve výhodě, tak hybridizuje celá smečka nespárovaných elektronů do jednoho tvaru orbitalu - a ten popisujeme kombinaci písmen všech hybridizovaných orbitalů - sp vs sd - viz závěr odkazovaného článku od
An analogous notation is used to describe sdx hybrids. For example, the permanganate ion (MnO4-) has sd3 hybridisation with orbitals that are 25% s and 75% d. Pauling also proposed combinations of s, p and d orbitals such as sp3d and sp3d2, but more recent calculations based on molecular orbital theory have shown that in main-group molecules the d component is insignificant, while in transition metal complexes the p component is insignificant (see below).
and see below и посмотри русскую таблицу.
Toto označení je třeba s paní učitelkou konzultovat - zda v zápisu má být zohledněn i d-orbital, který byl volný a posloužil pro umístění nespárovaného elektronu (v zápisu budou s, p, d), nebo v zápisu hybridizace jsou pouze elektrony z původní nabídky orbitalů (tedy jen s, p) bez ohledu, pomocí kterého orbitalu se pomohlo k uvolnění elektronových párů.
b) tvar molekuly - zkontroluj si podle tabulky - zakresli se pro každý vzorec, co máš.
H2SO3, H2SO4, H2S2O7 - Tu hybridizace mám špatně?
Hybridizace - zápis má přesně popsat všechny orbitaly účastné ve vazbě (a to až po excitaci). Síra v základním tvaru má pouze 2 samostatné elektrony p, zbytek je spárován. proto nejdřív excitujeme na orbital d a potom popíšeme, že hybridizace je sp3d (nebo sp3d2).
Vysvětluji si to tak - k dispozici sice mám pouze s, p elektrony, ale pošleme na d orbital, tedy výsledný tvar orbitalů musí být hybrid všech použitých orbitalů. Když d do zápisu nedám, tak není zřejmě, jaký výsledný tvar může hybridní orbital mít. Opět - upřesní si to s paní učitelkou.
HClO - Takže tvar neurčuji?
Určuješ - tato molekula by mohla být lineární, pokud by nebylo párů elektronů, díky kterých se linearita "zlomí"
HClO2, HClO3 -
takže HClO2 bude mít hybridizaci sp2 a tim pádem tvar molekuly bude lineární (+ dva volné elektronové páry)?
Cl opět musí mít v zápisu hybridu d-orbitál. Bude to lineární, ale lomena
u HClO3 nemůžu najít chybu
- opět d-orbitál do zápisu.
HClO4 - Nedokážu vytvořit excitovaný stav. Vždy, když vytvářím excitovaný stav, koukám se kolik má celkem vazeb. Zde je to
což je dohromady 4. V excitovaným stavu se vždy snažim docílit toho, abych měl dohromady ve všech "čtverečcích" pouze 4 samostatné elektrony.
"H-O-Cl-(3 dvojné vazby na 3 kyslíky)" - tedy Cl potřebuje celkem 7 nespárovaných elektronů. V základním stavu má pouze 1, proto "rozlepí" všechny dvojice s a p a dostane celkem 7 volných - zkus barevně.
HBO2 - Moc nechápu. Já topiž vždy zapíšu počet osamocených elektronů, které mi tam zůstanou. Po škrtnutí mi tam zůstanou jenom dva osamocené elektrony, tak moc nechápu proč sp2
- opět zapsala bych hybridizaci v excitovaném stavu
HPO3 - Ano, už vidim tu chybičku :-). Tedy hybridizace je sp2?
sp3d
H3PO4 Jinak je to vše správně?
sp3d
HNO2 Takže i přesto, že tam je pí vazba, škrtat elektrno nemusím?
- proč ho škrtáš - jaký to má význam pro další krok v pomocném papíru?
Určuje se tedy pak i tvar molekuly?
- vždy se určuje (dle tabulky)
HCN - Určitě vim, že jsou tam
a pak je tam tedy i jedna
.
Určitě tam 3 sigmy nejsou :-)
Každá jednoduchá čárka, která je samostatně, je vazba "sigma" (viz definice této vazby), pokud je vazba násobná (=), potom jedna je vždy "sigma", další už "pi". je to dáno možnosti orientace orbitalů v prostoru. Proto mezi H-C je vazba sigma, C-N v trojné vazbě je vazba sigma, "zůstatek" z trojné vazby C=N jsou 2 vazby pi.
Offline
#15 24. 02. 2013 12:59 — Editoval Vladislav97 (24. 02. 2013 13:23)
- Vladislav97

- Místo: Praha
- Příspěvky: 421
- Škola: Gymnázium
- Pozice: Student (Druhák)
- Reputace: 13
Re: Strukturní vzorce (domácí procvičování No. 1/3)
↑ jelena:
Děkuji za podrobné rozepsání :-)
Celková potíž s hybridizací
Nám to totiž profersorka vysvětlovala trochu jinak. A to tak, že v excitaci nejdřív musim osamostatnit elektrony podle počtu vazeb (klasický postup). A pokud se ve struktruním vzorci nacházaejí alespon nějaké vazny "pí", tak je automaticky škrtám v excitovaném stavu (kolik vazeb "pí", tolik elektronů škrtnu). A výslednou hybridizací bude excitovaný stav se škrtnutými elektrony (postup, který nám vysvětlila).
Např.
-Jedná "pí" vazba -> proto škrtám elektron -> a výslednou hybdridizaci zapisuji.
-Pak hledám molekulu takovou aby měla tři vazby + jeden volný elektronový pár. Což je pouze v tetraedru-> Trigonální pyramida. A pak si v tom řádku ověřim, jestli se to shoduje s hybridizací ->sp3
-Na druhou stranu, pokud budu mít sp3d (nebo sp3d2), tak v řádku s oktaedr-em, žádnou molekulu, která by měla tři vazby + jeden volný elektronový pár nenajdu.
Závěr:
Nevím tedy, musim opravdu zapisovat celý excitovabný stav s ("pí" vazbami), což je logičtější, anebo bez "pí" vazeb, kde se na druhou stranu shoduje tvar molekuly s hybridizací.

HClO4 - Nedokážu vytvořit excitovaný stav. Vždy, když vytvářím excitovaný stav, koukám se kolik má celkem vazeb. Zde je to
což je dohromady 4. V excitovaným stavu se vždy snažim docílit toho, abych měl dohromady ve všech "čtverečcích" pouze 4 samostatné elektrony.
"H-O-Cl-(3 dvojné vazby na 3 kyslíky)" - tedy Cl potřebuje celkem 7 nespárovaných elektronů. V základním stavu má pouze 1, proto "rozlepí" všechny dvojice s a p a dostane celkem 7 volných - zkus barevně.
--> Rozumím jáe jsem sčítal sigma a ´"pí" vazby, přičemž jsem měl sigma vazby špatně :-).
Takže pokud chápu správně. Když má někde trojnou vazbu  , tak je to jedna sigma (to je jasný)(
, tak je to jedna sigma (to je jasný)( ) a 2 "pí" (
) a 2 "pí" (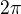 )?
)?
Děkuji moc :-). Podívám se ještě na ty doporučené knížky. Přeji hezký den :-).
P.S. Ted se dívám do té knížky a koukám, že je tam úplně ta samá tabulka, jakou nám dala :-)
Offline
#16 24. 02. 2013 15:07
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: Strukturní vzorce (domácí procvičování No. 1/3)
↑ Vladislav97:
:-) no konečně je to jasné - děkuji :-)
Já popisuji stav atomu ještě před vznikem vazby, Ty popisuješ stav atomu v molekule a správně popisuješ, že se atom "hybridně tváří" vůči vytváření stejných vazeb - vazeb "sigma". Tedy takovým systémem ještě jednou projdi své papíry - jestli jsem tento systém nenabourala a je všechno srozumitelné.
Celou dobu totiž se věnuji excitovanému stavu atomu, ale před vytvářením vazby (teď už škrtání dává smysl i mne).
Takže pokud chápu správně. Když má někde trojnou vazbu
, tak je to jedna sigma (to je jasný)(
) a 2 "pí" (
)?
ano, je to tak.
P.S. Ted se dívám do té knížky a koukám, že je tam úplně ta samá tabulka, jakou nám dala :-)
ano, také jsem tak došla na doporučení Klikorky - vybavovala, kde jsem tento styl viděla (a tuto učebnici jsme používali dost).
Offline
#17 24. 02. 2013 15:18
- Vladislav97

- Místo: Praha
- Příspěvky: 421
- Škola: Gymnázium
- Pozice: Student (Druhák)
- Reputace: 13
Re: Strukturní vzorce (domácí procvičování No. 1/3)
↑ jelena:
:-) tak to je dobře, že je to vše vyřešeno! Sám si ještě procvičim ty zbylý sady (narozdíl od kyselin, jsou to už soli). Snad se mi ten zítřejší test vydaří.
Děkuji moc za VELKOU pomoc a přeji hezký zbytek dne :-)
Offline
#18 24. 02. 2013 21:46
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: Strukturní vzorce (domácí procvičování No. 1/3)
↑ Vladislav97:
také děkuji a také za přání (zbytek dne (a nejen) byl věnován úklidu po výměně stoupaček (a nejen) - tedy hezký byl, vážně :-) Zítra přeji zdar v testu.
Offline
Stránky: 1
- Hlavní strana
- » Chemie
- » Strukturní vzorce (domácí procvičování No. 1/3) (TOTO TÉMA JE VYŘEŠENÉ)