Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 12. 04. 2013 17:17 — Editoval Yeax (12. 04. 2013 17:18)
Acidobazické vlastnosti sloučenin
Hoj, rád bych poprosil o polopatické vysvětlení proč je odpověď za b)Cu(NO3)2 správná v této otázce: Vyberte sloučeninu, která ve vodném roztoku reaguje slabě kysele:
a) MgF2 b) Cu(NO3)2 c) K2(COO)2 d) NaHCO3
d - uhličitá kyselina, jelikož je slabá, bude ve vodě disociovat do prvního stupně a to ne všechny své molekuly, kdežto silná zásada jako je Na disociuje pravděpodobně všechny své molekuly, tedy bude převažovat zásaditost ve výsledném roztoku... Jak bych si toto mohl zdůvodnit na samotné hydrolýze? H2CO3 + H2O -> HCO3- + H3O+ (vznikají oxoniové kationty v malém mmnožství, koncentrace OH- bude převažovat?)
NaOH + H2O -> ?
c - opět slabá kyselina se silnou zásadou, to stejné o řádek výše
b - vůbec netuším jak poznat, jak reaguje Cu(2+) s H2O, k. dusičná zřejmě odštěpí většinu svých H+ za vzniku velkého počtu H3O+
a - tady jsem opět úplně ztracen, HF je mám pocit nejslabší halogenovou kyselinou, jak reaguje hořčík ve vodě vůbec netuším...
Výše zmiňovaná otázka je z loňského přijmacího testu na LF MU.
Obecně jsem v této problematice dost slabý, takže kdyžtak při vysvětlování (byly by jste moc hodni :-)) na to berte zřetel :D. Dík
Offline
#2 12. 04. 2013 23:36
Re: Acidobazické vlastnosti sloučenin
Zdravím,
Máte v tom zmatek. Ve vodném roztoku soli probíhá disociace, obecně lze psát B jako kation, A jako zbytek kyseliny: 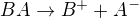 Kationty s1 a s2 prvků s vodou nereagují, zůstávají netečné. Stejně tak anionty silných kyselin. Naopak anion slabé kyseliny (A-) může reagovat s vodou takto:
Kationty s1 a s2 prvků s vodou nereagují, zůstávají netečné. Stejně tak anionty silných kyselin. Naopak anion slabé kyseliny (A-) může reagovat s vodou takto:
Podobně kation slabého hydroxidu (obecně B+):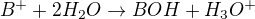
Stačí takto, či byste potřeboval i tyto konkrétní případy?
Doučím M, Ch v okolí Pardubic
Press any key to continue. Alt + F4?
Offline
#3 13. 04. 2013 00:21 — Editoval Yeax (13. 04. 2013 00:22)
Re: Acidobazické vlastnosti sloučenin
Chápu tu pointu, ale i tak bych to asi potřeboval ukázat na konkrétních příkladech.
Např. u onoho NaHCO3 se molekula disociuje na HCO3- a Na+.
Kation silné zásady s vodou reagovat nebude (proč?). To znamená, že reagovat bude pouze HCO3-. Jelikož kyselina uhličitá je slabá, do druhého stupně reagovat nebude, záchová se tedy aniont HCO3- jako zásada a přijme H+ od vody, což zapříčiní zvýšení koncentrace OH- a výsledný roztok poté bude zásaditý?
Cu(NO3)2 se bude štěpit na Cu2+ a NO3-. NO3-, aniont silné kyseliny, s vodou reagovat nebude. Cu + H2O -> Cu(OH)2 + H3O+, ve výsledném roztoku budou převažovat oxoniové kationty, roztok bude kyselý?
K2(COO)2 je postaveno na stejném principu jako ten hydrogenuhličitan sodný?
MgF2 - dočetl jsem se, že ve vodě je nerozpustný, tedy nemůže disociovat, říkám to správně? Teoreticky, kdyby mohl, tak F- je aniont slabé kyseliny a Mg s2 prvek - nebude reagovat. Ve výsledném roztoku by tedy byla opět převaha zásaditých hydroxylových aniontů?
Offline
#4 13. 04. 2013 21:44
Re: Acidobazické vlastnosti sloučenin
Tak jest.
Kationty s1 a s2 prvků nereagují s vodou, protože (vybetre si nejsrozumitelnější zdůvodnění):
*mají elektronovou konfiguraci vzácného plynu, v důsledku čehož jsou nereaktivní
*jsou vysoce neušlechtilé, tudíž jim forma volného kationtu vyhovuje
*mají nízkou elektronegativitu, tudíž nechtějí vstupovat do vazby, protože by se tím zvýšila elektronová hustota na kationtu
*kolem kationtu se vytvoří tzv. hydratační obal - molekuly vody se uskupí kolem kationtu, který je pak pro reaktanty nedostupný
(Ony tyto kationty reagují, ale v tak malé míře, že to lze zanedbat bez projevu na setinách stupně pH)
Doučím M, Ch v okolí Pardubic
Press any key to continue. Alt + F4?
Offline
#5 14. 04. 2013 10:46 — Editoval Yeax (14. 04. 2013 10:49)
Re: Acidobazické vlastnosti sloučenin
Řekl bych 4. možnost. Nicméně kolem d prvků se onen obal poté nevytváří, protože kation mědi v onom příkladu nahoře s vodou reagoval za vzniku hydroxidu. Proč tedy u s prvků vznikne a u d ne?
A neměly by právě z důvodů vysoké neušlechtilosti právě ony, stojící úplně vlevo beketovovy řady mít schopnost vytěsnit vodík z vody?
S vodou nereagují ani anionty silných kyselin, které úplně disociují, to si zdůvodním prosím jak?
Offline
#6 17. 04. 2013 23:19
Re: Acidobazické vlastnosti sloučenin
Zaprvé, kov a kation kovu je rozdíl asi jako nabitá a vybitá puška. Přesdtavte si Na jako nabitou a Na+ jako vybitou.
Zadruhé, u d prvků vstupuje do problému koordinační chemie. Molekuly vody se díky volným orbitalům vážou na kov, ale celý proces je celkem složitý, nezabíhal bych do něj.
Anionty silných kyselin s vodou sice reagují, mezi protonovanou a neprotonovanou formou je rovnováha. Síla kyselin je o tom, jak moc je přítomna deprotonovaná fotma vůči protonované.
Doučím M, Ch v okolí Pardubic
Press any key to continue. Alt + F4?
Offline
#8 18. 04. 2013 20:42
Re: Acidobazické vlastnosti sloučenin
↑ Yeax:
Není zač. V případě hlubšího zájmu doporučuju zkouknout letošní chemickou olympiádu kategorie B:
http://web.natur.cuni.cz/cho sekce Aktuální ročník - úlohy - 49skolni_zadani.pdf
Doučím M, Ch v okolí Pardubic
Press any key to continue. Alt + F4?
Offline
#9 18. 04. 2013 20:50
Re: Acidobazické vlastnosti sloučenin
Jinak celkem zajímavě se chová taková H3PO4. Při pH pod jeden bude ve zcela protonované formě, tedy H3PO4. Při pH okolo 5 bude ve formě H2PO4-, když pH zvýšíme na 10, tak bude ve formě HPO42-. Až pH nad třináct dokáže z H3PO4 odtrhnout všechny protony. Na toto byla celkem hezká praktická úloha právě v letošním ročníku ChO, ovśem v praxi.
Doučím M, Ch v okolí Pardubic
Press any key to continue. Alt + F4?
Offline

