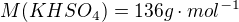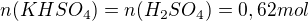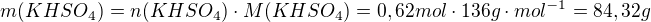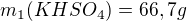Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 25. 05. 2013 11:11
Výpočet z rovnice
Určité množství 20% kyseliny sírové neutralizováno 42,7 gramu uhličitanu draselného. Po zahuštění vykrystalizovalo 66,7 gramu KHSO4. Vypočítejte výtěžek KHSO4 v %.
Nemůžete mi poradit aspoň s tou rovnicí, prosíííííím? :D
Offline
- (téma jako vyřešené označil(a) Bajiji)
#3 25. 05. 2013 13:48
Re: Výpočet z rovnice
↑ bismarck:
Děkuji..a jak by byl ten výpočet potom prosím?? Já vůbec nevím...Jenom jsem zjistila, že toho draslíku je tam 24,13 g...
Offline

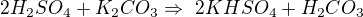
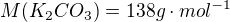
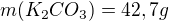
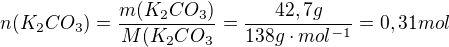
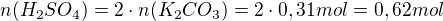
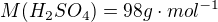
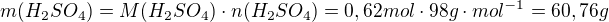
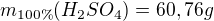
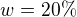
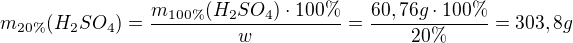 Nepriama úmera
Nepriama úmera