Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 29. 05. 2013 14:09
- starmatulik
- Příspěvky: 72
- Reputace: 0
Jaká je hmotnost vyloučené mědi?
Prosím o pomoc s příkladem, při elektrolýze vodného roztoku CuSO4 prošlo elektrolyzérem 0,010 molu elektronů. Jaká je hmotnost vyloučené mědi? [M(Cu) = 63,55 g/mol]
a) 0,32 g - správně
b) 0,64 g
c) 1,6 g
d) 3,2 g
2 CuSO4 + 2 H2O --› 2 Cu + O2 + 2 H2SO4
z rovnice:
2moly CuSO4.... 2 Cu
0,01 ......... x --> x=0,01
m(Cu)= n*M= 0,01*63,55=0,6355 , což je špatně, určitě se něco děje s těmi elektrony
katoda: 2 Cu+2 + 4e- --› 2 Cu
anoda: 2 SO4-2 + 2 H2O - 4 e- --› 2 H2SO4 + O2 , ale nevím, jak to zapsat do výpočtu..
Offline
- (téma jako vyřešené označil(a) starmatulik)
#2 29. 05. 2013 14:32 — Editoval rleg (29. 05. 2013 14:38)
Re: Jaká je hmotnost vyloučené mědi?
↑ starmatulik:
Finta bude v tom, že mědi chybí 2 elektrony, tudíž na vyloučení 1 molu mědi jsou potřeba 2 moly elektronů. Myslím, že na tohle ani není třeba psát rovnici reakce.
Radim, tedy jsem.
Dobrá rada je drahá, ta moje je zdarma.
Offline
#3 01. 10. 2013 14:33 — Editoval ChArOn (01. 10. 2013 14:35)
Re: Jaká je hmotnost vyloučené mědi?
Jak bylo naznačeno v předchozím případě, vše souvisí s látkovým množstvím prošlých elektronů.
Výpočet pak je dobré sestavovat z rovnice redukce kovu na katodě: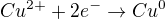
Pro výpočet pak sestavíte rovnici rozsahu chemické reakce: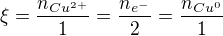
Pak do rovnice dosadíte správný vzorec pro výpočet hmotnosti mědi: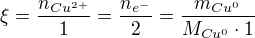
a po dosazení správných čísel 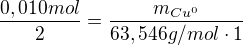
Vám vyjde hmotnost mědi: 0,3177 g.
Offline
