Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 01. 05. 2013 16:14
plyny
V tlakové nádobě o objemu 10 litrů je kyslík pod tlakem 1 MPa. V druhé nádobě o
polovičním objemu je vodík. Jaký musí být tlak vodíku, aby hustota obou plynů
v nádobách byla při dané teplotě stejná?
Prosím o pomoc s výpočtem, tak nějak nevím, kde začít s úvahou. Asi bych vyšel z rovnice pro izotermický děj, ale nějak nevím, jak tam zapojit tu hustotu. Ke správnému výsledku se mi podařilo dojít vypočtem přes molární hmotnost, ale to mi přijde tak silně nereálné jako správný postup, že to tu radši ani nebudu zbytečně dávat.
Děkuju
Offline
#2 01. 05. 2013 16:32
Re: plyny
Úvahu začni u stavové rovnice pro plyn (pV=nRT). Počet molů n lze vyjádřit jako podíl hmotnosti a molární hmotnosti. Když to uděláš, tak už není problém stavovou rovnici upravit tak, aby se tam vyskytoval jen tlak, konstanta R, hustota (podíl hmotnosti a objemu), teplota a molární hmotnost ... No a když takto upravíš obě rovnice (pro oba plyny) a dosadíš do nich všechny známé hodnoty, tak uvidíš že zjistit tlak v druhé nádobě už není problém. K cíli vedou i jiné úpravy, takže pokud ti to vyšlo dobře, tak by si to ani nemusel mít špatně, kdyžtak ten postup přece jenom napiš a uvidíš
Offline
#3 01. 05. 2013 17:07
Re: plyny
No takhle nějak jsem zprvu také uvažoval, jenže bych asi potřeboval správně pochopit zadání. Pokuď mám uzavřenou nádobu, nemůže přece dojít ke změně objemu plynu, tedy ani hustota se nemůže v rámci regulování teploty měnit, měl by se kvůli ní pouze měnit tlak plynu na stěny nádoby. Dále, z konce zadání mi není jasné, zdali při dané teplotě znamená, že teplota obou plynů musí být ve výsledku stejná stejně jako jejich hustota, nebo ne.
Kdybych v tomto měl jasno, hned by to šlo lépe... V té stavové rovnici po úpravě stále neznám teplotu T, samozřejmě, pokud ze zadání nevyplývá, že je konstantní.
Offline
#4 01. 05. 2013 17:46
Re: plyny
↑ Yeax: Zadání je myšleno takto. V jedné nádobě je kyslík, a ve druhé, která je úplně mimo je ten vodík. V obou nádobách je stejná teplota. No a právě z té stavové rovnice je vidět, jak spolu všechny ty údaje souvisejí a že se to všechno navzájem ovlivňuje. Taky si všimni, že ani nemáš zadáno kolik té látky v té nádobě má být. Takže v podstatě jde o to vyřešit tuto úlohu (pokud ti to bude připadat srozumitelnější) - Jestliže do druhé nádoby o polovičním objemu umístim takové množství vodíku, aby byla stejná hustota jako ve vedlejší nádobě, a poté nádobu seřídím na stejnou teplotu, na jaké hodnotě se ustálí tlak???
Offline
#5 01. 05. 2013 19:06
Re: plyny
Dobře.
Takže: M(kyslík)p(kyslík)=róRT => ró=Mp(kyslík)/RT=Mp(vodík)/RT => p(vodík)=Mp(kyslík)/M(vodík)
Výsledek je opravdu stejný jako správný uvedený výsledek u příkladu, tedy 16MPa.
V případě, že by jeden z prvků netvořil dvouatomové molekuly (např. místo vodíku by byl Neon), je správné počítat u kyslíku s dvouatomovou molekulou (řekl bych, že ano) nebo s jednoatomovou, tak jako u Neonu?
Offline
#6 01. 05. 2013 19:43
Re: plyny
Doporučovla bych když sem něco píšeš tak použít LaTexový editor, jinak se to hrozně blbě luští, ale vypadá to správně. Jinak když se koukneš na to řešení, tak to nevypadá, že by počet atomů v molekule ovliňoval výsledek. Samozřejmě kdyby molekula byla tvořena atomy různách prvků tak by to bylo něco jiného.... Protože molární hmotnost látky je vztažena na počet atomů a né molekul, tak v tomto případě to nemá na úlohu vliv
Offline
#8 11. 06. 2013 22:01
- Lachtanisko34

- Zelenáč
- Příspěvky: 1
- Reputace: 0
Re: plyny
nké složitosti něčem naprosto jednoduchám hledá velké složitosti takže zvolím li řešení úlohy úvahou...zvolím cestu zprávnou...pokud mi jedna látka(téměř ideální plyn) o molární hm. 16 x 2 = 32 prostoru logicky pro látku která má téměř stejné vlastnosti a molární hm 1 x 2 = 2 bude zabírat 16 menší plochu, pokud tedy budu druhou látku chtít nahustit stejně jako látku první musím použít 16x větší tlak než u první látky...tím mi výjde tlak 16 MPa nemusím nic počítat jen se na to úlohu dlouho zadívat :D je to logické?...je to děj izotermický pV=nRT pV=konst R=konst. n je 16 vyšší u kyslíku a T nedosazuji...tak co chcete počítatat?...vlastně jsem si musel vynásobit i molekuly plynu abych měl s čím počítat :D
Offline
#9 12. 06. 2013 12:26
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: plyny
↑ Lachtanisko34:
Zdravím,
i když nějakou ideu k možnému řešení nabízíš, máš moc formálních a neformálních nesmyslu, např.
pokud mi jedna látka(téměř ideální plyn) o molární hm. 16 x 2 = 32 prostoru logicky pro látku která má téměř stejné vlastnosti a molární hm 1 x 2 = 2 bude zabírat 16 menší plochu,
plyn (nejen ideální) má tu (ne)dobrou vlastnost, že zaplní celý objem, který je mu k dispozici (navíc je rozdíl "zabírat objem" nebo "zabírat plochu"). No atd. také je dobré si přečíst po sobě - např. nedostatek interpunkce snižuje čitelnost. Cesta zprávná je potom spíš cesta zrádná.
-----------------------------------
Jinak když se koukneš na to řešení, tak to nevypadá, že by počet atomů v molekule ovliňoval výsledek. Samozřejmě kdyby molekula byla tvořena atomy různách prvků tak by to bylo něco jiného.... Protože molární hmotnost látky je vztažena na počet atomů a né molekul, tak v tomto případě to nemá na úlohu vliv
jen pro upřesnění: látkové množství 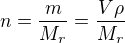 . Počet a skladba atomů v molekule ovlivňuje jen molární hmotnost, která je pro každou plynnou látku bude jedinečná z důvodu jedinečné skladby molekuly plynu. Pokud je zadán název plynu (chemický vzorec), jde o tabulková data. Klidně tuto úlohu můžeme modifikovat na O2 a CO2 místo H2.
. Počet a skladba atomů v molekule ovlivňuje jen molární hmotnost, která je pro každou plynnou látku bude jedinečná z důvodu jedinečné skladby molekuly plynu. Pokud je zadán název plynu (chemický vzorec), jde o tabulková data. Klidně tuto úlohu můžeme modifikovat na O2 a CO2 místo H2.
Offline
#10 12. 06. 2013 15:07
Re: plyny
↑ Lachtanisko34:
Zdravím
Já osobně bych chtěl jenom upozornit, že podobné úvahy (když je samozřejmě správě zformuluješ) jsou sice pěkné a mnohdy zkrátí cestu k výsledku, nicméně většinou nejdou považovat za korektní postup.
Jak v matematice, tak ve fyzice by ses měl opírat o fakta, nikoli o intuici, ať už vedou ke stejnému výsledku či nikoli. Tento problém je více výrazný v matematice (např. je spoustu jednoduchých tvrzení, které jsou z hlediska selského rozumu samozřejmá, nic méně korektní a přesné zdůvodnění je až neuvěřitelně složité). Chci tedy říci jen to, že se ti v budoucnu klidně může stát, že někdo kdo bude kontrolovat tvojí práci takovéto řešení prostě a jednoduše neuzná.
Ještě malé rýpnutí :) - říkáš "nemusím nic počítat jen se na to úlohu dlouho zadívat" - tak jak je možné, že když si se na tu úlohu dlouze díval, tak jsi si nevšiml že v zadání je napsáno, že má druhá nádoba poloviční objem??
Offline