Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 12. 10. 2013 01:21
chemická rovnováha
Zdravím, potřebuji lehce pomoct. Máme zadanou nějakou rovnici, na levé straně je dejme tomu kyselé prostředí, na pravé voda a máme otázku např. "Když zvýšíme zásaditost, tak a) rovnováha se nezmění b) rovnaváha se vychýlí k výchozím reaktantům c) rovnováha se vychýlí k produktům."
postupuji správně, když uvažuji, že zvýšením zásaditosti snížíme kyselost, to znamená zmenšíme koncetraci H+ na pravé straně a podle zákona chemické rovnováhy tedy snížíme koncentraci pravé strany, abychom zachovali konstantu? Tudíž se nám rovnováha vychýlí směrem k výchozím reaktantům?
jinak s tím souvisí další trochu hloupá otázka. Když se sníží koncentrace produktů, tak to bereme, že se rovováha vychýlí směrem k reaktantům, ok? Když se koncetrace produktů zvýší, tak to je asi jasné, rovnováha se vychýlí směrem k produktům.
A do třetice, když je otázka formulována pro zvyšování/snižování tlaku, tak si musím určit na které straně je víc plynných složek a od toho se pak odvíjí úvahy? Např. víc plynů je napravo, tlak zvýšíme, takže rovnováha se vychýlí směrem k produktům.
Pokud jsou mé úvahy chybné, byl bych rád kdyby mi někdo ten princip vysvětlil. Díky...
Offline
- (téma jako vyřešené označil(a) Svářeč)
#2 12. 10. 2013 15:42
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: chemická rovnováha
Zdravím,
používáš princip Le Chatelier - tak?
zmenšíme koncetraci H+ na pravé straně
asi na levé? Jinak se závěrem souhlasím.
Když se sníží koncentrace produktů, tak to bereme, že se rovováha vychýlí směrem k reaktantům, ok? Když se koncetrace produktů zvýší, tak to je asi jasné, rovnováha se vychýlí směrem k produktům.
To si ještě promyslí.
když je otázka formulována pro zvyšování/snižování tlaku, tak si musím určit na které straně je víc plynných složek a od toho se pak odvíjí úvahy? Např. víc plynů je napravo, tlak zvýšíme, takže rovnováha se vychýlí směrem k produktům.
úvaha by se měla odvíjet od faktu, zda při reakci dochází ke změně objemu plynných složek (látkové množství plynu nalevo a napravo v reakci). Pokud nedochází, tak vliv neposuzujeme.
A odvozujeme tak, jak jsi napsal, ale nedokončil - pokud látkové množství (objem produktů) je menší, než reaktantu, tlak v systému klesá. Tedy navýšením tlaku rovnováha jde směrem k produktům.
Např. víc plynů je napravo, tlak zvýšíme, takže rovnováha se vychýlí směrem k produktům.
to znamená, že reakce jde s růstem tlaku (v uzavřeném reakčním systému je více plynů), pokud tlak ještě zvýšíme, tak rovnováha jde směrem k reaktantům.
Myslím, že si musíš uvědomit, že posuzujeme nejdřív systém ve stavu rovnováhy. Potom tu rovnováhu změníme zvenku a hledím, jak systém zareaguje. On zareaguje tak, aby změnu potlačil. Je to tak přehledné? Děkuji.
Offline
#3 12. 10. 2013 20:18 — Editoval Svářeč (12. 10. 2013 20:20)
Re: chemická rovnováha
jelena napsal(a):
zmenšíme koncetraci H+ na pravé straně
asi na levé? Jinak se závěrem souhlasím.
Jo, popletl jsem to, samozřejmě na levé. Takže podle toho zákona (díky, takhle jsem to znění neznal) nám systém chce doplnit ztracené H, rovnice běží zpětně => rovnováha se vychyluje směrem k reaktantům. Už je to jasné, díky.
Tím pádem je jasné i to další - je to přesně naopak, než jsem to napsal. Ubereme produkty -> systém je chce doplnit -> rovnováha se vychýlí k produktům. Atd.
S tím tlakem mi tedy není jasná jedna věc - jak spočítám, kde je větší látkové množství plynu? Ze zákl. vzorečku 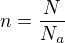 ? (S tím že av. konstantu můžeme asi vynechat, když to počítáme na obou stranách...?)
? (S tím že av. konstantu můžeme asi vynechat, když to počítáme na obou stranách...?)
Jinak u toho příkladu jsem zase popletl strany, jinak to asi chápu :) Máme větší objem plynu nalevo -> tlak při reakci klesá. Zvýšíme ho a aby systém zvýšený tlak eliminoval, rovnováha se posouvá k produktům, aby tlak klesnul.
Díky, pomohla jsi mi, akorát teda ještě prosím pomoct s tím určením množství plynu.
Offline
#4 12. 10. 2013 23:44
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: chemická rovnováha
↑ Svářeč:
také děkuji, řekla bych, že ten princip je dost přehledný - viz například úklid - sotva vznikne volný prostor, hned se musí zaplnit nepořádkem :-)
jak spočítám, kde je větší látkové množství plynu?
z vyčíslené rovnice reakce - jako příklad je hodně populární syntéza NH3 (reaktantů dle reakce 1+3 mol plynů, produktů jen 2 mol), pokud je jiné vstupující množství, tak vždy je úměrné vyčíslené reakci.
V tom se určitě zorientuješ, na VŠCHT jsou hodně dobré a dostupné materiály.
Offline
#5 12. 10. 2013 23:54
Re: chemická rovnováha
Aha, takže čistě podle počtu molekul, díky :) Všcht má hodně dobré materiály, jak skripta, tak různé internetové pomůcky (zvlášť předmět Ob. a an. chemie I, kterého se tohle týká), ale tohle jsem nějak nebyl schopný dohledat.
Offline
#6 13. 10. 2013 09:38
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: chemická rovnováha
↑ Svářeč:
tak co jiného by v uzavřené nádobě s plynem vytvářelo tlak, než molekuly plynu, že ano :-)
Tato problematika je podrobněji zařazována do Fyzikální chemie (u vás např. pro bakaláře), v 1. ročníku však ještě není dostatečný matematický aparát, proto se bere spíš slovně, potom se ještě doplní, ale určitě to můžeš číst. Pokud je všechno vyřešeno, označ, prosím, témata. Děkuji.
Offline