Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 27. 11. 2013 21:57
Teplená výměna (změna)
Dobrý večer,
potřeboval bych poradit s tímto příkladem:
Mám za úkol určit výslednou teplotu, přičemž platí následující - Čaj, jehož hmotnost se rovná 250g (250ml) o teplotě 100 C, je v železném skleničce o stejné teplotě jako čaj a s hmotností 500g. Do této skleničky dodíme 5 kostek ledu o hmotnosti 100g a teplotě -20
C, je v železném skleničce o stejné teplotě jako čaj a s hmotností 500g. Do této skleničky dodíme 5 kostek ledu o hmotnosti 100g a teplotě -20 C.
C.
Problém mám v tom, že jsou zde tři hodnoty měrné teplené kapacity, takže netuším jak to dát dohromady.
Za případnou pomoc, děkuji.
Offline
#2 27. 11. 2013 22:05
- marnes

- Příspěvky: 11227
Re: Teplená výměna (změna)
↑ tng013:
Je potřeba si uvědomit že
1) led se nejdříve musí ohřát na 0 stC
2) pak se led musí přeměnit na vodu o teplotě 0 stC
3) pak se tato voda ohřívá a čaj chladí
1-3 teplo přijímá a bere ho od čaje
Teplo přijate se musí rovnat teplu odevzdanému - musíš sestavit rovnici
Musíš si najít měrnou tepelnou kapacitu ledu a železa (snad čaj je stejná jako voda)
a měrné skupenské teplo tání
Jo. A na začátku vás zdravím.
Offline
#5 27. 11. 2013 22:58
Re: Teplená výměna (změna)
↑ marnes:
Vždyť ano, zjistil jsem si měrné tepelné teplo ledu (334 kJ*kg^-1) a pomocí toho vypočítal skupenské telo: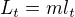
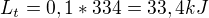 což je teplo potřebné ke změně skupenství, jestli se nepletu
což je teplo potřebné ke změně skupenství, jestli se nepletu
A pomocí této rovnice bych měl zjistit teplo potřebné ke změně teploty z -20 stC na 0 stC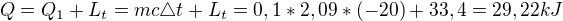
Omlouvám se, ale fyzika mi nikdy moc nešla. Stále nechápu jak mám zjistit výslednou teplotu po vhození kostek ledu do čaje ve skleničce. :/
Offline
#6 28. 11. 2013 09:43 — Editoval marnes (28. 11. 2013 09:44)
- marnes

- Příspěvky: 11227
Re: Teplená výměna (změna)
Tak jsem vypočítal, že je potřeba cca 29kJ tepla na změnu teploty ledu na 0 stC
je informace jen o 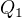
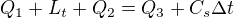
Q1 - teplo které přijme led při změně z -20 na 0 stC
Lt - přeměna ledu na vodu při teplotě 0stC
Q2 - ohřátí vody z 0 stC na výslednou teplotu t
Q3 - teplo odevzdané čajem ( vodou)
Cst - teplo odevzdané kalorimetrem ( skleničkou)
Cs - tepelná kapacita kalorimetru (skleničky)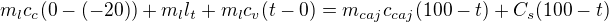
krom výsledné teploty vše znáš nebo musíš najít v tabulkách
Jo. A na začátku vás zdravím.
Offline