Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 03. 12. 2013 16:55
pH zmiešaného roztoku
Mám vypočítať pH roztoku, ktorý vznikne zmiešaním 0,5dm3 HNO3 s koncentráciou 10mol/dm3 a 0,1dm3 KCl s koncentráciou 5mol/dm3.
Som už trerí deň v pH výpočtoch a tento príklad ma zastavil
Offline
- (téma jako vyřešené označil(a) jelena)
#2 03. 12. 2013 20:04
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: pH zmiešaného roztoku
Zdravím,
KCl je sůl silné kyseliny a silné zásady, tedy nebude mít vliv na obsah H+ (nebo OH-) v roztoku, nepodléhá hydrolýze.
Ovšem přidáním "0,1dm3 KCl s koncentráciou 5mol/dm3" došlo ke zředění původního roztoku kyseliny, třeba vypočíst novou molární koncentraci HNO3 v roztoku a z toho odvodit pH. Podaří se tak dokončit? Děkuji.
Offline
#5 03. 12. 2013 20:19
Re: pH zmiešaného roztoku
↑ jelena:
použijem vzťah c1.V1 + c2.V2=c(V1+V2)
vychádzam z faktu, že mám dve rôzne látky, dve koncentrácie, dva objemy. Vypočítam teda koncentráciu roztoku, ktorý vznikne zmiešaním látok.
Môže byť? Ďakujem veľmi pekne za odpoveď
Offline
#6 03. 12. 2013 23:12
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: pH zmiešaného roztoku
↑ ivankaCH:
počítáme koncentraci kyseliny HNO3 ve výsledném roztoku, jelikož roztok KCl "přispívá jen objemem, ale žádnou kyselinu neobsahuje, 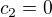 (zde nemůžeme brát koncentraci KCl). Pokud jsi tak myslela, potom může být.
(zde nemůžeme brát koncentraci KCl). Pokud jsi tak myslela, potom může být.
c1.V1 + 0.V2=c(V1+V2)
Offline
#7 04. 12. 2013 10:18
Re: pH zmiešaného roztoku
Dobrý deň stále nerozumiem. Mám príklad:
Jaké pH má roztok vzniklý smísením 30 cm3 roztoku HNO3 o koncen-traci 0,05 mol.dm-3 s 20 cm3 roztoku KOH o koncentraci 0,1 mol.dm-3?
a) 2
b) 3
c) 12
d) 10
správna odpoveď je c
a
284. Jaké pH má roztok vzniklý smísením 20 cm3 roztoku HCl o koncen-traci 0,1 mol.dm-3 s 30 cm3 roztoku NaOH o koncentraci 0,05 mol.dm-3?
a) 5
b) 2
c) 12
d) 11
správna odpoveď je b
Nemôžte mi prosím napísať Vašu myšlienkovú úvahu. Vôbec sa neviem pohnúť. Ďakujem a posielam sms na podporu
Offline
#8 04. 12. 2013 11:06
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: pH zmiešaného roztoku
↑ ivankaCH:
Zdravím,
to jsou typově úplně jiné příklady (ale je možné, že v úvodním příspěvku máš s KCl překlep). V dalších úlohách ↑ příspěvek 7: jde o reakce neutralizace, třeba zapsat, vyčíslit a pH stanoviš podle té látky, která bude v roztoku v přebytku (a koncentrace bude na celkový objem roztoků po smíšení).
KCl ale nereaguje s kyselinou, jen ředí roztok. Budeš tomu tak rozumět - i rozdílu úloh? Děkuji.
Offline
#10 04. 12. 2013 18:35
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: pH zmiešaného roztoku
↑ ivankaCH:
vyčíslené to je, ale třeba pokračovat. Reakce (stechiometrie 1:1) je v případě, že reaguje 1 mol a 1 mol (nebo tomu úměrné množství), potom bude prostřední neutrální. Ale jaké množství s kterým reaguje u Tebe v úloze?
smísením 30 cm3 roztoku HNO3 o koncen-traci 0,05 mol.dm-3 s 20 cm3 roztoku KOH o koncentraci 0,1 mol.dm-3?
Děkuji.
Offline
#11 04. 12. 2013 20:23
Re: pH zmiešaného roztoku
Ďakujem
Vypočítala som látkové množstvo HNO3: 0,05x0,03=1,5*10na3, vypočítala som látkové množstvo KOH: vyšlo mi 0,2*10na 3
Zistila som teda, že v zmesi HNO3 a KOH je HNO3 v nadbytku.
Je to zatiaľ dobrá úvaha?
Ak áno, ako zistím pH zmiešaného roztoku?
Offline
#12 05. 12. 2013 00:23
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: pH zmiešaného roztoku
↑ ivankaCH:
ano, zatím dobře (čísla jsem podrobně nekontrolovala - myslím, že máš chybu ve výpočtu, ale myšlenka v pořádku). Mně vyšlo, že v přebytku je KOH, ještě překontroluj.
Ale budu používat Tvé čísla, pro samotný princip je to jedno. Tedy víme, že 0,2*10^-3 mol HNO3 se vyčerpalo na reakci, v roztoku máme (1,5-0,2)10^-3 mol HNO3.
Jelikož jsme roztoky smíchali, můžeme použit, že 1,3*10^-3 mol HNO3 je teď v 50 cm^3 roztoku a stanovit molární koncentraci, následně pH.
Offline
#13 05. 12. 2013 13:32
Re: pH zmiešaného roztoku
Dobrý deň, urobila som si to poctivo, asi chápem princíp ale nevyšlo mi to, niekde robím chybu. Prosím, veľmi chcem rozumieť tomuto príkladu a napíšem vám môj postup:
Jaké pH má roztok vzniklý smísením 30 cm3 roztoku HNO3 o koncen-traci 0,05 mol.dm-3 s 20 cm3 roztoku KOH o koncentraci 0,1 mol.dm-3?
a) 2
b) 3
c) 12
d) 10
1. vypočítam si n(HNO3): c x V= 0,03dm3 x 0,05 = 0,0015mol
2. vypočítam si n(KOH): c x V = 0,02 dm3 x 0,1 = 0,002 mol
3. porovnala som n(HNO3) a n (KOH) a zistila som, že mám KOH v prebytku.
4. z toho mi vyplýva, že som na reakciu vyčerpala celé množstvo HNO3 a v roztoku mi zostalo už len 0,0005mol KOH
5. vypočítala som molárnu koncentráciu tak, že som použila vzťah: c = n/V
6. dosadila som za n rozdiel látkových množstiev a za V celý objem roztoku, čiže 0,0005mol/0,05dm3 = 0,01
7. ak je c = 0,01, potom pH mi vyšlo 2
Správna odpoveď však má byť 12. Nechápem, ďakujem
Offline
#14 05. 12. 2013 13:57
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: pH zmiešaného roztoku
↑ ivankaCH:
děkuji, jsi šikovná :-)
Chybu nevidím, ovšem z molární koncentrace KOH vypočteš pOH, tedy ještě krok pH=14-2. V pořádku? Děkuji.
Offline
#16 05. 12. 2013 23:33
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: pH zmiešaného roztoku
↑ ivankaCH:
také děkuji, úžasná ani ne, jen opravdu potěší podpořit takovou snahu:
Prosím, veľmi chcem rozumieť tomuto príkladu a napíšem vám môj postup:
Ať se vede v přípravě (patrně na medicinu nebo přírodovědné obory).
Offline
