Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 11. 02. 2014 14:16 — Editoval Harry (11. 02. 2014 15:21)
příklad kontrola
Zdravím, prosím o kontrolu příkladů:
1. Vodík se v laboratoři připravuje reakcí zinku s kyselinou chlorovodíkovou. Kolik gramů Zn a kolik ml 36% roztoku HCl (ρ= 1,1789 gcm-3) je třeba na přípravu 50 dm3 H2 (za st. p.)?
Mr(HCl)= 36,5 Mr(Zn)= 65,4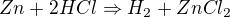
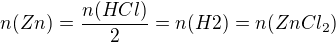
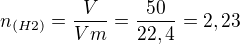

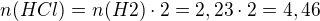
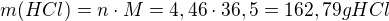
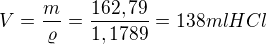
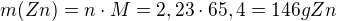
2. Jaká je hmotnost 1∙10^25 molekul CO2? Jaký objem toto množství zaujímá za standardních
podmínek? Mr(CO2)= 44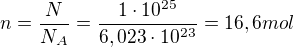


3. Vypočtěte, jaký je za standardních podmínek objem 8,5.10^23 molekul H2, jakou hmotnost má toto množství H2?


Offline
#7 11. 02. 2014 20:08
Re: příklad kontrola
↑ Harry: (1 mol hoci aj 6-atomoveho plynu zaberá stále len 22.4 dm3.) Tam sa na vnútro nehľadí.
**********************
Pozerám ale, že som prehliadol aj v dvojke chybu :-( ... 1 mol zaberá 22.4 litra=22.4 dm3 ...!!! tak nie mililitre!!
pozor tak si oprav prosím... aj trojku... nie mililitre... ale dm3
Offline
#9 12. 02. 2014 17:36
Re: příklad kontrola
↑ Harry: Takže objemy sú už v poriadku aj 2. aj 3.
a ako som predtým uviedol, aj keď budeš mať plyn N2O5 = 7 atomov tak do stavovej rovnice dáš len 1 mol a dostaneš 22.4 litra. 1mol vo veľkom našom ľudskom priestore zodpovedá
v mikrokozme 1 molekule (=7atomov).
Tu je pôvod 22.4dm3 na 1mol.
http://www.wolframalpha.com/input/?i=10 … V%3DnRT%22
Tých 7 atomov je tak natesnaných k sebe do malého priestoru, že sa pri nárazoch na stenu správajú ako jednoatomový plyn. ako jedna pevná nedelitelná častica. Je to divné, ale zhruba sa to tak uznáva. Samozrejme sú drobné odchýlky, ktoré sa prejavujú v extrémnych podmienkach. (Ale tam našťastie sa netlačíme, tak fajn).
Offline

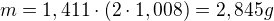 a V by mělo být správně.
a V by mělo být správně.