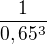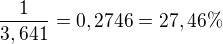Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 02. 06. 2014 20:18
Reakcni kinetika
Potrebovala bych prosim pomoct s timto prikladem, vubec nevim co s tim:
Rychlost reakce 2A + B = C závisí na koncentraci takto: v = k * cA(na druhou) * cB. Vypočtete na kolik procent počáteční rychlosti klesne rychlost reakce v okamžiku, kdy zreagovalo 35% látky A. Na počátku reakce je reakční směs tvořena látkami A a B ve stechiometrickém poměru.
Dekuji
Offline
#2 02. 06. 2014 22:13
Re: Reakcni kinetika
↑ roxen:
Zdravím.
Bylo by dobré si vyjádřit aktuální koncentrace A a B v momentě, kdy zreaguje 35% látky A jako násobky počátečních koncentrací. Pak dosadit do rychlostní rovnice a výsledek bude zřejmý.
Napište, čemu konkrétně nerozumíte.
Doučím M, Ch v okolí Pardubic
Press any key to continue. Alt + F4?
Offline
#4 03. 06. 2014 10:16
Re: Reakcni kinetika
Je to v podstate uloha na diferencialne rovnice. Rychlost reakcie:![kopírovat do textarea $v=-\frac12\frac{\mathrm{d}[a]}{\mathrm{d}t}=-\frac{\mathrm{d}[b]}{\mathrm{d}t}$](/mathtex/39/39a47a0a9b70f13f2b4527c8145b8d1a.gif)
kde okamzite koncentracie znacim hranatymi zatvorkami; ked su latky na zaciatku v stechiometrickom pomere, tak v nom budu vzdy pocas reakcie: ![kopírovat do textarea $[a]=2[b]$](/mathtex/24/2447feae33c23a0a5ad39acec2f9e877.gif) , tym padom
, tym padom![kopírovat do textarea $v=4k[b]^3=-\frac{\mathrm{d}[b]}{\mathrm{d}t}$](/mathtex/65/65195f7597ba35afe4e82595627ab134.gif)
![kopírovat do textarea $\int_{c_{B,0}}^{c_B}[b]^{-3}\mathrm{d}[b]=-\int_0^T{4k\mathrm{d}t}$](/mathtex/18/1860d9bb52575b13fb8f0cfef83488dd.gif)
kde 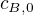 je pociatocna koncentracia latky B a
je pociatocna koncentracia latky B a 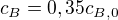 je koncentracia v momente ked ju chceme zistit; kvoli stechiometrickemu pomeru je jedno ci berieme latku B alebo A
je koncentracia v momente ked ju chceme zistit; kvoli stechiometrickemu pomeru je jedno ci berieme latku B alebo A![kopírovat do textarea $\left.-2[b]^{-2}\right|_{c_{B,0}}^{c_B}=-2\frac{1}{c_B^2}+2\frac{1}{c_{B,0}^2}=-4kT$](/mathtex/b4/b46cca3d8f35272f77ee579ebdd7e61d.gif)
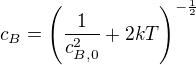
a cas 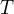 za ktory to nastane:
za ktory to nastane: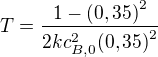
Vidime, ze ten cas zavisi aj na pociatocnej koncentracii.
Offline
#7 22. 06. 2015 19:23
Re: Reakcni kinetika
↑ Johi:
Kolega ↑ Xellos: tu řešil něco, co nebylo v zadání.
Pokud máme rychlost reakce definovanou takto: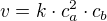
tak číslo "o kolik se zmenší rychlost" bude podíl počáteční a momentální rychlosti. Na počátku je rychlost takováto: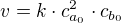
Po zreagování 35 % reaktantu A (a tedy i 35 % reaktantu B, jelikož jsou ve stechiometrickém poměru) dostaneme rychlost takovouto: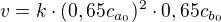
Zvládnete to dořešit?
Doučím M, Ch v okolí Pardubic
Press any key to continue. Alt + F4?
Offline