Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 12. 06. 2014 13:30 — Editoval jelena (12. 06. 2014 15:20)
- monika4419

- Příspěvky: 98
- Reputace: 1
elektrolyt
Proč není octan sodný ve vodném roztoku slabý elektrolyt?
Pochází ze slabé kyseliny - octové 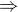 měl by být slabý elektrolyt
měl by být slabý elektrolyt
Offline
- (téma jako vyřešené označil(a) monika4419)
#2 12. 06. 2014 13:31
- monika4419

- Příspěvky: 98
- Reputace: 1
Re: elektrolyt
↑ monika4419:↑ monika4419:
*měl by být slabý elektrolyt
Offline
#3 12. 06. 2014 15:23
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: elektrolyt
Ještě pozdrav - pokud chceš zvýraznit některou část testu, tak např. do
Code:
[b]...[/b]
dostaneš tučné písmo (podrobně). Na druhou stranu v úloze máš sůl silné zásady, tedy rozhodování podle slabé kyseliny nemusí být směrodatné.
Offline
#4 13. 06. 2014 00:45
Re: elektrolyt
Takto to nefunguje. Sila kyseliny hovori ako velmi kyselinovy anion pritahuje 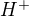 (cim silnejsia, tym menej), nie ako velmi pritahuje
(cim silnejsia, tym menej), nie ako velmi pritahuje 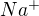 (a to cim lepsie, tym horsie sa vo vode rozpusta). Pri elektrolytoch je podstatne kolko uvolni do roztoku latka ionov; v tomto zmysle je octan sodny dobry elektrolyt, pretoze sa rozpusta strasne dobre, takze v roztoku bude ionov vela. A preco sa neskombinuju aniony kyseliny s kationmi
(a to cim lepsie, tym horsie sa vo vode rozpusta). Pri elektrolytoch je podstatne kolko uvolni do roztoku latka ionov; v tomto zmysle je octan sodny dobry elektrolyt, pretoze sa rozpusta strasne dobre, takze v roztoku bude ionov vela. A preco sa neskombinuju aniony kyseliny s kationmi 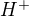 ? Pretoze (ak sme tam pridali octanu slusne mnozstvo) tych v roztoku vela nebude. Hlavne tam budeme mat aniony octanove a kationy sodne, a kazdeho priblizne tolko kolko sme tam nahazdali octanu.
? Pretoze (ak sme tam pridali octanu slusne mnozstvo) tych v roztoku vela nebude. Hlavne tam budeme mat aniony octanove a kationy sodne, a kazdeho priblizne tolko kolko sme tam nahazdali octanu.
Skratka: podstatna pre vodivost roztoku soli je hlavne rozpustnost soli, nie sily kyseliny a zasady, z ktorych bola vyrobena.
Offline
#5 13. 06. 2014 08:55
Re: elektrolyt
↑ Xellos:
Zdravím, ale oni se octanove anionty skombinuji. I kdyby se měly kombinovat s vodou:
AcO- + H2O = AcOH + OH-.
Nicméně těch záporných vodivych iontů tam bude pořád stejně.
Doučím M, Ch v okolí Pardubic
Press any key to continue. Alt + F4?
Offline


![kopírovat do textarea $10^{-4,76}=\frac{[A^-][H^+]}{[AH]}$](/mathtex/d5/d5c14156d4835deb6946e0c0bc61f823.gif)
![kopírovat do textarea $[H^+]=10^{-9}$](/mathtex/46/46a149434c07f2da8b00c407cfde78be.gif) ,
,![kopírovat do textarea $\frac{[A^-]}{[AH]}=10^{-4,76+9}=2\cdot10^4$](/mathtex/87/872e0336db02a476f82cca6651c27776.gif)
![kopírovat do textarea $K = \frac{\[AcOH\] \cdot \[OH-\]}{\[AcO-\]} \nl
K_w = \[H+\] \[OH-\] \Rightarrow \[OH-\] = \frac{K_w}{\[H+\]} \nl
K = \frac{\[AcOH\] \cdot K_w }{\[AcO-\] \cdot \[H+\]} = \frac{K_w}{K_a} \nl
\[AcOH\] = \[OH-\] \nl
\frac{1}{K_a} = \frac{K_w }{\[AcO-\] \cdot \[H+\]^2}\nl
K_a =\frac{\[AcO-\] \cdot \[H+\]^2}{K_w } \nl
pK_a = 2pH -\log \[AcO-\] - pK_w \nl
pH= \frac12 (pK_w + pK_a + \log\[AcO-\])$](/mathtex/8b/8b7912b4750daa96d22118a3292d8443.gif)