Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 13. 06. 2014 20:27 — Editoval klokie (13. 06. 2014 20:38)
příklad na neutralizaci
dobrý večer!
prosím jak si poradit s příkladem: k neutralizaci 30 ml roztoku NaOH se spotřebovalo 40 ml roztoku H2SO4 (c=0,1 mol/l). vypočtěte koncentraci hydroxidu.
rovnice je 2 NaOH + H2SO4 ---> Na2SO4 + 2 H2O
V=30 ml V=40ml
c=x c=0,1 mol/l
logicky si myslím, že 40*0,1 by mělo mít stejnou hodnotu jako 30*x, ale to mi nesedí s výsledkem... :(
Offline
- (téma jako vyřešené označil(a) klokie)
#2 13. 06. 2014 20:53
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: příklad na neutralizaci
logicky si myslím, že 40*0,1 by mělo mít stejnou hodnotu jako 30*x
:-) no tak, jsme v sekci Chemie, jaké "logicky myslím"?
Reakci máš dobře a podle reakce reaguje dvojnásobný počet mol NaOH oproti počtu mol H2SO4. Také platí, že 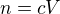 , teď to použij pro výpočet.
, teď to použij pro výpočet.
Offline
#3 13. 06. 2014 20:59
Re: příklad na neutralizaci
↑ jelena:
aha, to už s výsledkem sedí! takže jsem si vypočítala látkové množství kyseliny, to pak vynásobila dvěma, protože reagoval dvojnásobný počet molů hydroxidu oproti kyselině. to jsem pak zase zpětně dosadila do vzorečku a vypočítala koncentraci. už to chápu. :) děkuji!
Offline
#4 13. 06. 2014 23:17
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: příklad na neutralizaci
↑ klokie:
:-) šikovná (a při správném vedení kolegy to jde ještě lépe, kolegovi děkuji).
Do úvodního tématu jsem sbírala celkem použitelné odkazy, možná něco použiješ.
Offline