Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 03. 09. 2014 23:38
- siiimonka77
- Zelenáč
- Příspěvky: 5
- Reputace: 0
Zoxidování mědi
Ahoj,
mohl by mi prosím někdo pomoct s tímto příkladem?
Lodička s čerstvě vyredukovanou mědí má hmotnost 16,8 g. Oxidací kyslíkem narostla hmotnost
lodičky se směsí na 17,8 g.
a. Vypočítejte, z kolika % měď zoxidovala ?
b. Vypočítejte, kolik g CuO vzniklo za předpokladu, že hmotnost lodičky je 9,1 g a oxidací
se nemění.
rovnice reakce: 2 Cu + O2 2 CuO
Díky moc
Offline
#2 04. 09. 2014 08:36
Re: Zoxidování mědi
↑ siiimonka77:
Ahoj,
stačí si rozmyslet, jaké látkové množství ("kolik molů") představuje 1 gram kyslíku O2. Pak už by to mělo být vidět.
Доктор сказал «в морг» — значит в морг!
Offline
#3 04. 09. 2014 09:30
- siiimonka77
- Zelenáč
- Příspěvky: 5
- Reputace: 0
Re: Zoxidování mědi
↑ Formol:
Nemůžeš mi to prosím nějak napsat? :) mně to asi nedochází bohužel.:(
Offline
#4 04. 09. 2014 10:25
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: Zoxidování mědi
Zdravím,
Formol napsal(a):
stačí si rozmyslet, jaké látkové množství ("kolik molů") představuje 1 gram kyslíku O2. Pak už by to mělo být vidět.
Mám dojem, že budu nabízet trochu jiný postup (ale pokyn "rozmyslet" jsem se pokusila zrealizovat, no hm :-).
↑ siiimonka77:
znáš původní hmotnost mědi a hmotnost směsí "nezreagovaná měď a vzniklý CuO" po reakci s kyslíkem. Potom předpokládej, že reagovalo 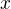 gramů Cu. Zkus vyjádřit teď (s použitím
gramů Cu. Zkus vyjádřit teď (s použitím 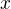 ), kolik g CuO vzniklo dle reakce a kolik mědi zůstalo nezreagováno.
), kolik g CuO vzniklo dle reakce a kolik mědi zůstalo nezreagováno.
Co se Tobě podařilo zatím poskládat? Děkuji.
Offline
