Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 16. 09. 2014 17:49
- obsidianen
- Příspěvky: 72
- Reputace: 0
Molární objem
Dobrý den, nechápu tenhle příklad:
Určete molární objem kyslíku o2 při teplotě 0 stupňů Celsia a tlaku 10 na pátou Pa, je-li hustota kyslíku za těchto podmínek 1,41 kg*m-3
Má vyjít Vm=22,7*10-3 m3*mol-1
Zjistila jsem, že molární hmotnost je součet relativních atomových hmotností Ar všech atomů vynásobený Avogadrovou konstantou a hmotnostní konstantou.
Ar pro o2 je teda 32 g/mol, což je 0,032 kg/mol
Dosadila bych do vzorce Vm=Mr/ ró
Šlo by to tak?
Offline
- (téma jako vyřešené označil(a) obsidianen)
#2 16. 09. 2014 19:53
Re: Molární objem
↑ obsidianen:
zdravím
šlo by to jednoducho zo stavovej rovnice ideálneho plynu: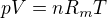 skade
skade 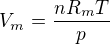
kde n je 1 pretože hľadáme molárny objem, čiže objem jedného molu. R_m je univerzálna plynová konštanta, ostatné hodnoty len treba dosadiť.
vyšlo mi to 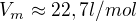 čo sa zhoduje.
čo sa zhoduje.
Per aspera ad astra
Offline
#3 16. 09. 2014 21:14
Re: Molární objem
Pořádek je pro blbce, inteligent zvládá chaos!
Offline
