Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 23. 11. 2014 21:14
Redoxní titrace 4
Prosím o pomoc s příkladem:
Navážka 3,0874 g kyzových výpalků byla rozpuštěna v kyselině a objem roztoku byl doplněn na 100 m. 10 ml tohoto roztoku bylo po redukci na železnatou sůl titrováno roztokem  o c = 0,01685 mol/l a spotřeba činila 33,65 ml. Vypočtěte obsah
o c = 0,01685 mol/l a spotřeba činila 33,65 ml. Vypočtěte obsah 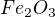 v procentech ve vzorku.
v procentech ve vzorku.
Látkové množství dichromanu mi vyšlo 0,000567 mol...z toho jsem vypočítala látkové množství železnatých iontů 0,000567 : 6 = 0,000945 mol. Nevim ale jestli je to dobře a výsledek mi pořád nevychází ..
Děkuji..
Offline
#2 23. 11. 2014 21:35
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: Redoxní titrace 4
Děkuji za označení (vidím, že zvládnuto), ještě jsi označila další úlohu bez reakce, tedy vyřešeno.
látkové množství železnatých iontů 0,000567 : 6 = 0,000945 mol.
toto je nejspíš zdroj problému - Fe(2+) je 6tinásobek (viz Tvá reakce), tedy násobit, ne dělit. Ozvi se, zda vychází. Děkuji.
Offline
#4 23. 11. 2014 23:53
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: Redoxní titrace 4
↑ Fčela:
toto je látkové množství Fe(2+), které vstupovalo do reakce s K2Cr2O7. Před tím ještě běžela reakce "redukci na železnatou sůl". tedy uvedené látkové množství Fe(2+) vzniklo při reakci z Fe(3+) (redukce). Tu ještě musíš sestavit a vyčíslit. Tak jdeš zpět od konečného analyzovaného produktu k úvodnímu vzorku, ve kterém bylo Fe2O3.
Pozor na ředění a koncentrace.
Offline
