Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 30. 11. 2014 00:50
Výpočet hm. % Síry
Zdravím , nemohl by mi prosím někdo pomoct s tímto příkladem ?
Vypočtěte, kolik hm. % síry obsahuje síran železitý.
Výsledek má být 24 % , ale vůbec netuším jak k tomu dojít .
Pak tu mám ještě jeden příklad
a) Vypočtěte, kolik kg 5% roztoku uhličitanu draselného musíte smíchat s 20% roztokem téže
látky, abyste získali 400 kg 10% roztoku uhličitanu draselného.
b) Vypočtěte látkovou (molární) koncentraci získaného 10% roztoku (ρ = 1,09 g/cm3
Pomůže někdo ? Děkuji
Offline
#2 30. 11. 2014 01:40 — Editoval ewer12 (30. 11. 2014 01:43)
Re: Výpočet hm. % Síry
První příklad:
(molární hmotnost budu značit M)
síran železitý = 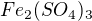
musíš zjistit poměr hmotnosti síry k celku, neboli 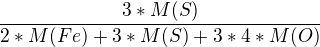
molární hmotnosti najdeš v periodické tabulce
Druhý příklad:
A)
uhličitan draselný = 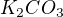
voda = 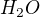
podle zadání příkladu musí platit: 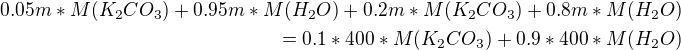
Kde m je hmotnost v kg, molární hmotnosti uhličitanu draselného a vody najdeš na internetu nebo vypočítáš podle periodické tabulky
B)
protože hmotnost/hustota = objem, můžeš napsat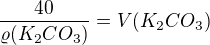
a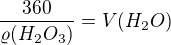
koncentrace C je tedy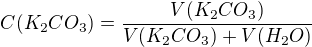
Nejsem si úplně jistý, jestli jsem někde neudělal chybu, tak si to raději zkus zkontrolovat, ale je z toho čitelný způsob, jakým jsem to řešil, tak snad tě to aspoň navede na správnou cestu k řešení takových příkladu. :)
Offline
#3 30. 11. 2014 08:41
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: Výpočet hm. % Síry
↑ ewer12:
Zdravím a děkuji,
bohužel 2. nebude dobře,
a) Při míchání roztoků s hmotnostní koncentraci máme směšovací rovnici 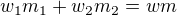 (
(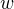 je hmotnostní zlomek (nebo může být všude hmotnostní % koncentrace bez převodu na hmotnostní zlomky),
je hmotnostní zlomek (nebo může být všude hmotnostní % koncentrace bez převodu na hmotnostní zlomky),  hmotnost roztoku. V rovnici nalevo jsou údaje pro jednotlivé roztoky - označeno indexem.
hmotnost roztoku. V rovnici nalevo jsou údaje pro jednotlivé roztoky - označeno indexem.
b)
protože hmotnost/hustota = objem, můžeš napsat
ano, zde (hmotnost roztoku)/(hustota roztoku) = objem roztoku (ρ = 1,09 g/cm3). m roztoku z předchozího kroku je 400 kg, použit převod jednotek a vypočíst objem roztoku V.
Potom - potřebujeme molární koncentraci, což je 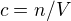 a vidíme, že musíme vypočítat
a vidíme, že musíme vypočítat 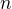 látkové množství
látkové množství 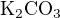 v jeho 10% roztoku.
v jeho 10% roztoku.
↑ Adam19: v 2. úvodním tématu sekce je hodně vzorových výpočtů + nedávej do tématu více úloh viz pravidla Ozvi se, zda jsi dopočítal. Děkuji.
Offline
#5 30. 11. 2014 12:37
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: Výpočet hm. % Síry
↑ ewer12:
Zdravím, nic se neděje (zejména, když chemii nemáte :-). Úlohy jsou opravdu ze základních pojmů na složení a na koncentrace, kolega to v úvodním tématu dohledá.
Jen k tomu to bych upřesnila
Tak by se mohl stanovit objemový zlomek, ale pouze za předpokladu, že součet objemu skutečně součtem (není složením ovlivněn). Např, kdybys počítal geometrickou úlohu, ve které se slepí kostka a jehlan ze stejného materiálu (bez dutin), nebo v přibližných výpočtech objemových % hodně ředěných kapalin (ale to už nekoréktní). Jinak říkáme, že sčítání objemů není aditivní, nelze obvykle použit - a příklad je "hrách a mák" (1 litr a 1 litr nedává 2 litry).
Zde máme pěknou ukázku, že na sčítání lze nachytat i takové autority :-)
Offline
