Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 18. 03. 2015 17:07 — Editoval Rendy77 (18. 03. 2015 17:12)
Molární koncentrace
Dobrý den,
potřebovala bych pomoci, nebo alespoň naťuknout, jak začít. Konkrétně jde o tento příklad:
Kolik 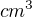 20% kyseliny chlorovodíkové (ρ = 1,098
20% kyseliny chlorovodíkové (ρ = 1,098 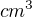 ) a kolik
) a kolik 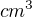 vody je třeba na přípravu 2 litrů jejího 1,117 M roztoku o hustotě 1,0181
vody je třeba na přípravu 2 litrů jejího 1,117 M roztoku o hustotě 1,0181 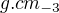 ?
?
Předem Vám moc děkuju..!
Offline
#2 18. 03. 2015 17:11 Příspěvek uživatele Rendy77 byl skryt uživatelem Rendy77.
#3 18. 03. 2015 20:22
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: Molární koncentrace
Zdravím,
dílčích postupů jak začít můžeš mít více. Podstatné je, že údaj "na přípravu 2 litrů jejího 1,117 M roztoku" přesně udává látkové množství HCl ve výsledném roztoku a toto množství musíš "najít" v původním roztoku 20% kyseliny.
Osobně bych postupovala tak, že 2 litry 1,117 M roztoku převedu (přes zadanou hustotu) na hmotnost roztoku a údaj o koncentraci (1,117M) přepočtu na hmotnostní koncentraci. Potom mohu sestavit směšovací rovnici v hmotnostních koncentracích. A dokončit převody hmotností roztoků na objemy.
Jiný způsob je stanovit molární koncentraci 20% roztoku a potom použit směšovací rovnici látkových koncentrací. V 2. úvodním tématu je dost takových úloh i s řešením. Kam se podařilo zatím dopočítat? Děkuji.
Offline
#5 22. 03. 2015 18:35 — Editoval jelena (22. 03. 2015 18:41)
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: Molární koncentrace
↑ Rendy77:
Také pozdravy :-)
m=81,54 g je hmotnost HCl v požadovaném objemu připravovaného roztoku, potom ve 20% roztoku to bude činit 20 % ("aktivní složka" roztoku) a celková hmotnost roztoku je 100 % 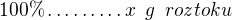
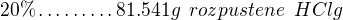
Souhlasíš? Výsledek je stejný, jen forma zápisu (u mne je úměra přímá, co znamená ta Tvoje nepřímá?), potom přepočet na objem, jak máš. Řekla bych, že v pořádku.
Offline
#7 23. 03. 2015 21:33
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: Molární koncentrace
↑ Rendy77:
my na to, že "v Chemii je prý vždy nepřímá úměra", považuji za naprosto převratný pohled na věc a ponořím se do hlubokých úvah o možných důsledcích takového světonázoru :-)
Ne, že bych nepochopila filosofii tvrzení: čím menší koncentrace roztoku (oproti 100% čisté látce), tím více toho roztoku má být, ale je to zajímavý pohled, když ho porovnám s definici procentuální (hmotnostní) koncentrace. Navrhuji ještě počkat na stanovisko kolegů, co v sekci aktivně působí. Kolegy zdravím.
Offline
#9 29. 03. 2015 19:19 — Editoval O.o (29. 03. 2015 19:22)
Re: Molární koncentrace
↑ Rendy77:
Nekontroloval jsem vysledky, ale rikate, ze je mate stejne.
Co se tyce neprima umera je v chemii vzdy, tak je to uplne mimo misu. Postup mate oba prakticky stejny, trojclenku muzes postavit na stejny problem primo i neprimo, jedine na cem potom zalezi je, jaky mate myslenkovy pochod. Tvoje musi jit neprimou umerou, jinak by to nedavalo smysl, stejne tak musi jit jeleny trojclenka primou umerou, protoze by jinak proste nedavala smysl.
U trojclenky si na zacatku nerikej, jestli ji udelas primou umerou nebo neprimou, to je preci zavisle na tom, jak dany problem resis, tady ted sam vidis, ze stejny problem je mozne resit primou i neprimou umerou. Co si musis rict je jak postupujes.
Kdyz bych mel roztok 20% latky X a redil ho (tj. zvetsoval objem jinym roztokem bez latky X), tak musim nakonec logicky dostat roztok o mensi koncentraci nez na pocatku - to je trojclenka.
20% ..... 1 dm3
x% ........ 2 dm3
---------------------
Umera je to neprima, ale ne proto, ze to rekla ucitelka ve skole, ale protoze redeni (viz. vyse) zvetsi celkovy objem, ale nezvetsi mnozstvi latky, tedy koncentrace se musi snizit.
Pri tvoreni trojclenky se vzdy zamysli nad tim, jak by to melo logicky byt, zbytecne papouskovat, co ti nekdo rika nepovede ke vzdy spravnemu vysledku ;-).
Offline
#10 31. 03. 2015 00:25
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: Molární koncentrace
Zdravím,
↑ O.o: děkuji za zapojení do tématu :-) Teď jsem si rozmyslila, že již u sestavení trojčlenky odříkávám tak, že je vidět, jaké je to úměra. A dosud jsem (snad) neuvažovala, že stejnou úlohu mohu napsat jako přímou i jako nepřímou úměru (viz zde v tématu), nebo "klasika ohledně kopáčů": 5 kopáčů za 2 měsíce, za jak dlouho stejný výkop 10 kopáčů?
Pro nepřímou:
5 kopáčů .... 2 měsíce,
10 kopáčů... x měsíců.
Pro přímou: doplním práci za časovou jednotku, tedy 1/2 práce a 1/x práce. A je přímá:
5 kopáčů zvládnou 1/2 práce za měsíc
10 kopáčů zvládnou 1/x práce za měsíc.
Pokud jsem to v takto pozdní hodinu zvládla :-) ↑ O.o: Jinak využiji tématu k přivolání kolegy houbar(e) a také se podívej, jak funguje důsledek tlačítka Nahlásit (jelikož jsme to necvičili při moderátorském zácviku. Pro pořádek - manuál je tam viz také "pro Moderátory".
Offline
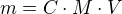
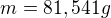
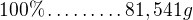
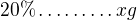
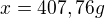

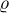 = ρ hustota
= ρ hustota