Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
Stránky: 1
- Hlavní strana
- » Chemie
- » Vyčíslování chemických rovnic - reakce MnS2 s PbO2 (TOTO TÉMA JE VYŘEŠENÉ)
#1 19. 11. 2015 18:36 — Editoval Bedlasky (19. 11. 2015 19:16)
Vyčíslování chemických rovnic - reakce MnS2 s PbO2
Dobrý den. Vkládám sem tuto redoxní rovnici, s kterou si nevím rady. Dnes jsem ji přepočítával a našel jsem si v ní jednu chybu, ale i tak mi nevychází.
Disulfid manganatý reaguje ve vodném roztoku kyseliny dusičné s oxidem olovičitým za vzniku síranu olovnatého, dusičnanu olovnatého a manganistanu olovnatého.
Zde je rovnice: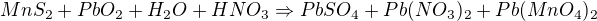
Zde jsou poloreakce:
Vzhledem k tomu, že na pravé straně rovnice vodík nefiguruje, doplnil jsem tam vodu. U oxidovaných iontů jsem elektrony sečetl a použil křížové pravidlo - dvojku jsem tedy doplnil k MnS2 a dvanáctku k PbO2. Poté jsem dopočítal na druhé straně rovnice síran a manganistan, podle zbylého olova jsem doplnil dusičnan, nalevo jsem podle dusičnanu doplnil kyselinu dusičnou. Výsledek vypadá potom takto:
Počet manganů, olova, dusíků a kyslíků mi sedí. Nesedí ale počet vodíků. Pokud tedy zvýším počet molekul vody na pravé straně rovnice, musím ale také zvýšit počet kyslíků na levé straně. A tady jsem ve slepé uličce. Dělám někde něco špatně? Mě osobně napadlo, jestli jsem neudělal chybu v poloreakcích. Jestli bych totiž neměl počítat s disulfidem jako: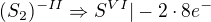
Děkuji za případné rady a pomoc.
Offline
- (téma jako vyřešené označil(a) Bedlasky)
#2 19. 11. 2015 19:23
Re: Vyčíslování chemických rovnic - reakce MnS2 s PbO2
↑ Bedlasky: Kolega Houbar minule upozornil...Co se vody týče:
když je někde kyselina nebo zásada, tak voda bude na opačné straně.
Dokážeme si to v našom prípade. Nechajme rovnicu tak ako si Ty napísal a matematika nám ju dá na správnu stranu.
a MnS2 + b PbO2 + c H2O +d HNO3 === e PbSO4 + f Pb(NO3)2 + g Pb(MnO4)2
Mn 1 0 0 0 0 0 2
S 2 0 0 0 1 0 0
Pb 0 1 0 0 1 1 1
O 0 2 1 3 4 6 8
H 0 0 2 1 0 0 0
N 0 0 0 1 0 2 0
6 rovnic...7 nezn.
We are done. RREF(A)=
1 0 0 0 0 0 2
0 1 0 0 0 0 19
0 0 1 0 0 0 -14
0 0 0 1 0 0 28
0 0 0 0 1 0 -4
0 0 0 0 0 1 -14
2 MnS2 + 19 PbO2 + -14 H2O +28 HNO3 === 4 PbSO4 + 14 Pb(NO3)2 + 1 Pb(MnO4)2
alebo teda preložíme vodu na pravú stranu lebo má koeficient znamienko mínus.
2 MnS2 + 19 PbO2 + +28 HNO3 === 4 PbSO4 + 14 Pb(NO3)2 + 1 Pb(MnO4)2 + 14 H2O
Offline
#3 19. 11. 2015 21:39
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: Vyčíslování chemických rovnic - reakce MnS2 s PbO2
Zdravím,
↑ Bedlasky: děkuji za založení samostatných témat.
Vodu, která má být jen napravo, jste již pořešili - viz kolega ↑ pietro:, děkuji.
Jestli bych totiž neměl počítat s disulfidem jako:
ano, počítala bych tak, jen 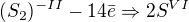 . Vychází? Děkuji.
. Vychází? Děkuji.
Offline
#4 19. 11. 2015 23:26
Re: Vyčíslování chemických rovnic - reakce MnS2 s PbO2
↑ jelena:
Děkuji za pomoc, opravdu to vychází! Jen se chci zeptat, proč tam máte dvakrát sírový kationt? Nás právě ve škole učili, že když tam mám nějaký prvek dvakrát (např.  ), tak počet elektronů potřebný z daného oxidačního čísla na výsledné (třeba z nuly na pět) násobíme dvěma (tedy 5*2). Vy jste ale udělala z -2 na 2*6, tedy na 12. Takže proto jsem to měl špatně a správný je Váš postup?
), tak počet elektronů potřebný z daného oxidačního čísla na výsledné (třeba z nuly na pět) násobíme dvěma (tedy 5*2). Vy jste ale udělala z -2 na 2*6, tedy na 12. Takže proto jsem to měl špatně a správný je Váš postup?
Jen ještě takový dotaz, když jsme třeba ve škole vyčíslovali nějakou reakci s peroxidem vodíku, tak jsme tam vždy dávali ke kyslíku oxidační číslo -1. Je to tedy špatně a měl bych správně zapisovat  ?
?
A když mám třeba v zadání, že látka A reaguje s látkou B v prostředí vodného roztoku látky C, jde už od začátku poznat, že voda má být na pravé straně rovnice? Vím, že třeba Houbar a Pietro zmiňovali, že v reakci kyseliny se zásadou bude voda vždy na druhé straně. Platí to ale vždy? Děkuji.
↑ pietro:
Vám také děkuji za pomoc. Jen se chci zeptat, tu soustavu jste počítal Gaussovou eliminační metodou?
Offline
#5 20. 11. 2015 12:05
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: Vyčíslování chemických rovnic - reakce MnS2 s PbO2
↑ Bedlasky:
Zdravím, já to mám zvyklé tak, že v těchto případech nebudu zapisovat jen Cl(0), ale celou molekulu
já to mám zvyklé tak, že v těchto případech nebudu zapisovat jen Cl(0), ale celou molekulu 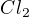 potom při sestavení bilance mi musí souhlasit nejen počet elektronu, ale také i počet atomů chlorů, tedy např. při přeměně Cl2 na HCl budu mít
potom při sestavení bilance mi musí souhlasit nejen počet elektronu, ale také i počet atomů chlorů, tedy např. při přeměně Cl2 na HCl budu mít 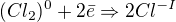 . Začínám urovnáním počtů atomů, nejdřív vynásobím 2 napravo, až potom počítám elektrony potřebné pro přechod.
. Začínám urovnáním počtů atomů, nejdřív vynásobím 2 napravo, až potom počítám elektrony potřebné pro přechod.
Tak naučili a zatím mi to fungovalo, ale ještě si počkej na kolegu houbar(e), měl by mít nejnovější poznatky a snad i zná dobrý odkaz.
Jen ještě takový dotaz, když jsme třeba ve škole vyčíslovali nějakou reakci s peroxidem vodíku, tak jsme tam vždy dávali ke kyslíku oxidační číslo -1. Je to tedy špatně a měl bych správně zapisovat
ano, tak bych napsala.
A když mám třeba v zadání, že látka A reaguje s látkou B v prostředí vodného roztoku látky C, jde už od začátku poznat, že voda má být na pravé straně rovnice? Vím, že třeba Houbar a Pietro zmiňovali, že v reakci kyseliny se zásadou bude voda vždy na druhé straně. Platí to ale vždy? Děkuji.
v některém předchozím příspěvku jsem také napsala, že bych vodu nepsala na obě strany, ale tak, aby šlo vyrovnat vodíky (zejména pokud vidím, že mi jedině voda urovná). Pokud si vybavuji, tak většina reakcí bude s vodou napravo.
Ještě snad pozor na zápis poloreakcí, kdy je velmi důležité prostředí, ve kterém reakce probíhá. Nejvíce toho posbíráš cvičením a "čtením" různých reakcí - dobrá sbírka je např. u pana Canova v Anorganice (nalevo v nabídce - potom rovnice, poloreakce, chemie prvků)
Offline
#6 20. 11. 2015 13:32
Re: Vyčíslování chemických rovnic - reakce MnS2 s PbO2
↑ Bedlasky:Ahoj, rád som, keď Ti to pomôže. Odkedy poznám
tzv.Gaussovu elim. metodu,
tak už nemám žiadne strachy z vyrovnávania rovníc.:-)
A ešte keď použijeme stroj
http://www.di-mgt.com.au/cgi-bin/matrix_canon_form.cgi
ktorý eliminuje ľudské chyby, tak sa celkom rýchlo dostaneme k cieľu.
Offline
#7 20. 11. 2015 14:20 — Editoval Bedlasky (20. 11. 2015 14:26)
Re: Vyčíslování chemických rovnic - reakce MnS2 s PbO2
↑ jelena:
Já si pak včera večer vlastně uvědomil, že jsem udělal v poloreakcích chybu. U toho disulfidu jsem zapomněl dát k síře dvojku. Pokud bych to počítal s tím oxidačním číslem -1, také by to mělo vyjít, ale musel bych to násobit dvěma. Ten Váš způsob mi ale přijde lepší, líbí se mi víc. V některých případech by ten můj způsob vyčíslování mohl i zkomplikovat řešení. Děkuji moc za pomoc :).
Offline
Stránky: 1
- Hlavní strana
- » Chemie
- » Vyčíslování chemických rovnic - reakce MnS2 s PbO2 (TOTO TÉMA JE VYŘEŠENÉ)
