Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#2 08. 12. 2015 00:25
Re: Látkové množství
↑ jáchym16:
Zdravím.
Takže, budeme vycházet z této rovnice: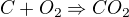
Nejdříve si musíme spočítat látkové množství kyslíku z tohoto vztahu: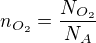
Dále si spočítáme hmotnost kyslíku: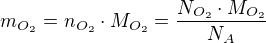
A nakonec si spočítáme hmotnost uhlíku - zase trojčlenkou, výslednou rovnici ale napíši obecně: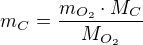
Můžeme to však také udělat jedním krokem a to, že si vytvoříme ze všech zmiňovaných vztahů jeden výsledný, kde dosadíme za hmotnost kyslíku 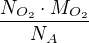 . Molární hmotnosti kyslíku se nám pokrátí a vznikne tento vztah:
. Molární hmotnosti kyslíku se nám pokrátí a vznikne tento vztah: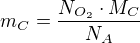
Offline
