Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#2 15. 12. 2015 20:18
Re: výpočet- vznik vodíku
↑ klokie:
Zdravím.
Vycházíme z této chemické rovnice:
Z objemu a normálového molárního objemu lze spočítat látkové množství: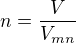
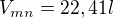
Hmotnost vodíku lze vypočítat z látkového množství a molární hmotnosti: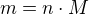
Nebo také můžeme z obou vztahů udělat jeden, tedy: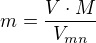
Poté si vypočítáme z trojčlenky hmotnost HCl potřebné k reakci (nezapomeňme na stechiometrické koeficienty), dále si spočítáme hmotnost chloridu zinečnatého a nakonec hmotnost zinku.
Offline
#3 15. 12. 2015 21:54 — Editoval klokie (15. 12. 2015 22:24)
Re: výpočet- vznik vodíku
↑ Bedlasky:
Můžete prosím rozepsat ten krok od trojčlenky?.. resp. vyšlo mi to 14,6, je to tak správně?
Offline
#4 20. 12. 2015 16:58
Re: výpočet- vznik vodíku
↑ klokie:
Omlouvám se, že píšu po takové době, všiml jsem si Vašeho příspěvku až dnes. Ano, Váš výsledek je správný.
Já jsem to počítal takto (od té trojčlenky):
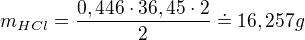

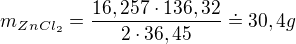

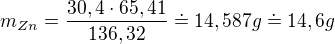
Předpokládám, že Váš postup byl stejný. Jsem rád, že jsem Vám pomohl :).
Offline
