Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#2 02. 02. 2016 12:29
Re: jak poznám, s čím reaguje zinek?
↑ klokie: Ahoj,
máme tu napr. odkaz od Jeleny :-), databáza reakcií
Odkaz
=========
V princípe všetko reaguje so všetkým, keď sa dostanú molekuly do blízkosti svojich orbitálov.
Nás zaujíma ale zrejme teraz vonkajší efekt, či je ten vzťah trvalý a "viditeľný".
=========
V databáze sú zaznamenané "viditeľné" reakcie.
Offline
#4 02. 02. 2016 16:26
Re: jak poznám, s čím reaguje zinek?
Reakcia prebehne v naznačenom smere viditelne (spontánne) len vtedy, keď
reaktanty su ochotné vzdať sa svojich doterajších vazieb a radšej vytvoria nové stabilnejšie produkty.
To je tak okrasne povedané.
Všetko je skryté v silách vazieb.
Asi preberáte potenciály elektrod, tak sa na to pozrime z tejto strany.
Ušlachtilé kovy sú preto šlachetné, lebo sú stále-odolné voči vonkajším podmienkam (Au). Nereagujú tak ľahko. Sú v tabulke elektrod. potenciálov
v kladnej oblasti
https://cs.wikipedia.org/wiki/Beketovov … _kov%C5%AF
Naproti tomu tie nešlachetné (Li) , tie by reagovali so všetkým až sa sami zničia.
Budem pokračovať neskôr, tak len narýchlo posielam odkazy..
Vysvetlenie Zn +NaCl
https://answers.yahoo.com/question/inde … 739AAcA7wb
A vzťahy medzi potenciálmi, rovnovážnou konštantou a Gibbs energiou
http://chemwiki.ucdavis.edu/Analytical_ … modynamics
Offline
#5 02. 02. 2016 20:35 — Editoval Bedlasky (02. 02. 2016 23:25)
Re: jak poznám, s čím reaguje zinek?
↑ klokie:
↑ klokie:
Zdravím. Stejně jako kolega Pietro soudím, že se asi ptáte na Beketovu řadu kovů.
https://cs.wikipedia.org/wiki/Beketovov … _kov%C5%AF
Najděte si v té tabulce zinek. Neušlechtilé kovy - tj. kovy s elektropotenciálem nižším než vodík, reagují s HCl. Tedy zinek bude reagovat s HCl za vzniku chloridu zinečnatého a vodíku.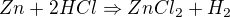
Dále platí, že když reaguje kov s nižším elektropotenciálem se solí kovu s vyšším elektroponteciálem, tak se kov s nižším elektropotenciálem oxiduje, zatímco kov s vyšším elektropontenciálem se redukuje. Takovou typickou reakcí je reakce železa se síranem měďnatým.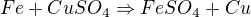
Toto však neplatí u žádné Vámi jmenované sloučeniny se zinkem. Sodík i hořčík mají nižší elektropotenciál než zinek, tudíž je zinek nemůže vytěsňovat z jejich solí.
Jinak, co jsem se díval na internet, tak jsem našel i reakci zinku s hydroxidem sodným. (Edit: Ještě jsem zapomněl dodat, že se jedná o amfoterní kov (to znamená, že dokáže vystupovat jako kyselina i jako zásada), reagující se silnými kyselinami i zásadami).![kopírovat do textarea $Zn + 2NaOH + 2H_{2}O\Rightarrow Na_{2}[Zn(OH)_{4}] + H_{2}$](/mathtex/33/33bf968b2a7723a5a0dbf390358c560f.gif)
Je to už jasnější?
Offline
