Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 15. 09. 2016 19:51
Výpočet hmotnostního zlomku
Mám takový dotaz na výpočet této rovnice:
Jaký bude hmotnostní zlomek chloridu sodného v soustavě, která vznikla neutralizací roztoku připraveného rozpuštěním 50g NaOH v 550 ml vody plynným chlorovodíkem?(0,113)
Začla jsem vytvořením rovnice a dále netuším, předem děkuji za odpověď
Offline
#2 15. 09. 2016 20:56 — Editoval Bedlasky (15. 09. 2016 20:56)
Re: Výpočet hmotnostního zlomku
↑ AleneZ:
Zdravím. Rovnici sem napíšu ještě jednou pro přehlednost.
Z jednoho molu NaOH vzniká 1 mol NaCl. Když se podívám na molární hmotnosti obou látek, zjistím kolik váží 1 mol dané látky. Trojčlenkou pak tedy mohu spočítat, kolik vznikne NaCl z 50g NaOH.
Obdobným způsobem vypočítáte hmotnost vody, která při reakci vzniknete a přičtete ji k hmotnosti vody, která byla v roztoku předtím. Následně si spočítáte hmotnost roztoku NaCl. Pak už stačí dosadit do tohoto vztahu: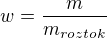
Offline
#3 17. 09. 2016 09:09
Re: Výpočet hmotnostního zlomku
↑ Bedlasky:
Taky to jde trochu jinak. Když se podíváme na rovnici, vidíme, že všechny vzniklé látky jsou kapalné (voda, rozpuštěné ve vodě).
Z rovnice vyplývá, že látky spolu reagují v poměru látkových množství 1:1, takže
n(NaOH) = n(HCl) = n(NaCl). Použijeme tedy vztah n = m/M a vypočítáme látkové množství NaOH:
n(NaOH) = 50/40 = 1,25mol. Použitý vztah upravíme do tvaru m = n*M:
m(HCl) = n(HCl)*M(HCl) = 1,25*36,5 = 45,6g
m(NaCl) = n(NaCl)*M(NaCl) = 1,25*58,4 = 73g
Hmotnost roztoku se zvýšila o pohlcený chlorovodík:
m(rozt.) = 550g vody + 50gNaOH + 45,6gHCl = 645,6g
w(NaCl) = 73/645,6 = ......
Offline

