Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 06. 11. 2016 18:31
Výpočet koncentrace z pH
Ahoj,
ve škole jsme dostali zadání na výpočet koncentrace kyseliny z pH=4,2 o molární hmotnosti 118,09 g/mol a pKa o hodnotě 5,2.
Mohli byste mi prosím pomoci? Zkoušel jsem to počítat přes ph= -log(cH+), jenže mi to sice vyšlo 0,0000623, ale nevím, co to vůbec vyšlo, zda to mám dobře nebo ne.
Děkuji za pomoc. :-)
Offline
#2 06. 11. 2016 18:52
Re: Výpočet koncentrace z pH
↑ flagman:
Zdravím,
vztah 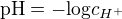 platí jen pro silné kyseliny. Pokud vám v úloze zadali pKa, pak se pravděpodobně jedná o kyselinu slabou, pro kterou se musí výsledek počítat z rovnováhy:
platí jen pro silné kyseliny. Pokud vám v úloze zadali pKa, pak se pravděpodobně jedná o kyselinu slabou, pro kterou se musí výsledek počítat z rovnováhy: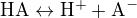
pro kterou je definovaná Ka jako
Po pár úpravách a zanedbáních (nejkřiklavější, že 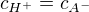 ) dostaneme tento známý vztah:
) dostaneme tento známý vztah:
Pokotýkám, že 
Stačí takto?
Doučím M, Ch v okolí Pardubic
Press any key to continue. Alt + F4?
Offline
#3 06. 11. 2016 19:36 — Editoval flagman (06. 11. 2016 20:07)
Re: Výpočet koncentrace z pH
↑ houbar:
Tak to jsem trochu nepochopil. Omlouvám se, ale mohl byste mi to trochu více osvětlit? Jsem asi tupý.
Děkuji. :-)
Pokud to chápu dobře, tak stačí vyjádřit ten logaritmus ze vzorce? Nebo je to úplně jinak?
Jestliže tomu tak je, tak mi vyšlo 0,3222. Je to správně?
Offline
#4 07. 11. 2016 09:53
Re: Výpočet koncentrace z pH
↑ flagman:
Běžně se používá pro výpočet pH slabých kyselin vztah
pH = 0,5*(pKa - log(ca)) kde ca je koncentrace slabé kyseliny. Z něj dostaneš
log(ca) = pKa - 2pH => ca = 10^(pKa-2*pH)
Je rozdíl ve výpočtech pro silné (pKa < 2), středně silné (2<pKa<4) a slabé (pKa>4) kyseliny. Zatím, co u silných kyselin je možné zanedbat podíl nedisociované kyseliny, a při přibližném výpočtu i vliv aktivit, zejména u nepříliš koncentrovaných roztoků, u slabých kyselin je možné zanedbat rozdíl mezi analytickou koncentrací a aktuální koncentrací kyseliny vlivem disociace. Platí to o nepříliš zředěných roztoků, protože stupeň disociace se zředěním a růstem pH může výrazně růst. U středně silných kyselin je nutné použít vztah pro disociační konstantu, při čemž uvažujeme i úbytek koncentrace kyseliny disociací. Současně u čistých roztoků jednosytných kyselin můžeme uplatnit vztah c(H+) = c(A-) a pak dostaneme
Ka = c(H+)^2/(ca - c(H+))
Tento vztah je poměrně univerzální, takže jej můžeme použít i pro slabé kyseliny pro výpočet Ka nebo ca (analytické koncentrace) kyseliny.
Ve tvém případě přibližný vztah, který uvádím nahoře vede k výsledku
ca = 10^(5,2 - 8,4) = 10^-3,2 = 6,3*10^-4mol/dm3
Přesnější vztah ca = c(H+)^2/Ka + c(H+) kde Ka = 6,31*10^-6 a c(H+) = 6,31*10^-5
ca = (6,31*10^-5)^2/6,31*10^-6 + 6,31*10^-5 = 6,94*10^-4 mol/dm3
OK?
Offline

