Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 17. 11. 2016 20:26
- lenuuuuska

- Příspěvky: 29
- Reputace: 0
Kyselina HF
Dobrý večer, chcela by som sa opýtať či súvisia vodíkové väzby s tÝm že HF je slabá kyselina..že tie vodíkové väzby pútajú k sebe častice. Ďakujem
Offline
#2 17. 11. 2016 21:36
Re: Kyselina HF
↑ lenuuuuska:
Ne zcela, zde se jedná hlavně o efekt polarizovatelnosti vazby.
Doučím M, Ch v okolí Pardubic
Press any key to continue. Alt + F4?
Offline
#3 18. 11. 2016 18:02
Re: Kyselina HF
↑ lenuuuuska:
Mám pocit, že trošku zaměňuješ příčinu a následek. Vazba H-F je velmi silně polární a navíc oba atomy jsou valmi malé, takže je malá i délka vyzby. Vazba je proto mimořádně silná, proto je HF slabou kyselinou. To je také důvod velkého dipólového momentu a tedy i tvorby poměrně silných vodíkových můstků. Sílu kyseliny navic snižuje to, že oba malé atomy jsou prakticky nepolarizovatelné, takže sílu vazby nesnižuje působení polárních molekul rozpouštědla, jak to vidíme u ostatních halogenvodíků, kde s rostoucím poloměrem atomu halogenu roste jeho polarizovatelnost s následným oslabením vazby a shora dolů pak snadnější disociací - tedy rostoucí sílou kyseliny.
Podobný efekt vidíme i v sousední 6. skupině PSP. Disociační konstanty chalkogenvodíků rostou shora dolů:
H2S -> H+ + HS- 1,22*10^-7; H2Se -> H+ + HSe- 1,28*10^-4 a H2Te -> H+ + HTe- 1,86*10^-4
Offline
#5 19. 11. 2016 16:01
Re: Kyselina HF
↑ houbar:
Je to ještě trochu jinak. To co píšeš, je Kw.
K = c(H+)*c(OH-)/c(H2O = 10^-14/55,5 = 1,802*10^-16; v Kw, stejně jako v Ka nebo v některých Kb se disociační konstanta od rovnovážné konstanty liší tím, že koncentrace vody je považována za konstantní a je převedena na levou stranu vztahů.
V zásadě máš pravdu, chci jen zdůraznit rozdíl mezi prostou rovnovážnou konstantou disociační reakce K a disociačními konstantami Ka, Kw nebo Kb.
Offline
#6 19. 11. 2016 21:38
Re: Kyselina HF
↑ Jozka2:
Tak tady se mýlíš ty. Konstanty rovnovážných reakcí se počítají z aktivit. Aktivita je taková zajímavá veličina, která u zředěných roztoků nabývá velmi podobných hodnot jako koncentrace. A aktivita vody je z definice jednotková, stejně jako aktivita jakékoliv pevné fáze. I kdybychom tam tu vodu tedy napsali, tak by to na velikost konstanty nemělo vliv.
Tímhle jsem si fakt jistý, pokud máš podobnou jistotu, pošli mi sem, prosím, zdroj.
Doučím M, Ch v okolí Pardubic
Press any key to continue. Alt + F4?
Offline
#8 20. 11. 2016 21:16
Re: Kyselina HF
↑ Jozka2:
C. E. Housecroft: Anorganická chemie (2014, překlad VŠCHT) na straně 202 potvrzuje moje teze. A teď si vyberte...
Dokonce píší: "...podle konvence je koncentrace vody jednotková, [H2O]=1"
Doučím M, Ch v okolí Pardubic
Press any key to continue. Alt + F4?
Offline
#9 20. 11. 2016 21:27
Re: Kyselina HF
↑ Jozka2: Kolegové Klikorka, Hájek a Votinský píší (s. 278, druhý díl přídílných skript Obecná a anorganická chemie): "Polohu rovnováhy vyjadřuje rovnovážná konstanta K=[H3O+].[OH-]. Konncentrace kapalné H2O ve vztahu nefiguruje, neboť je konstantní a je již zahrnuta do rovnovážné koncentrační konstanty"
Což v podstatě říkají trochu jinak to samé, a to, že rovnováhu autoprotolýzy vody vyjadřuje tato rovnice: K = c(H+)*c(OH-). Jinými slovy, disociační konstanty jsou jen dalším z typů rovnovážných konstant.
Doučím M, Ch v okolí Pardubic
Press any key to continue. Alt + F4?
Offline
#10 21. 11. 2016 16:25
Re: Kyselina HF
↑ houbar:
Naproti tomu skripta Bartoš, ....: Analytická chemie I (UPCE 2004) str. 62 a dál rozlišuje konstantu disociace vody K(H2O) = 1,8*10^-16 a iontový produkt vody Kw = 10^-14. Myslím, že tohle je korektnější, protože Kw je použitelné jen ve zředěných roztocích, kde koncentrace vody je blízká těm 55,6mol/dm3.
Je faktem, že někteří autoři používají úmluvu, že aktivita vody při teplotě 25°C je rovna 1, takže je to standardní stav. Není vyloučené, že jsou to nějaké dohody posledních 10-15 let.
Offline
#11 21. 11. 2016 23:41
Re: Kyselina HF
↑ Jozka2:
To jsou ti analytici, ti většinou fyzikální chemii moc neřeší. (ve skriptech UPCE r. 1987 je to taky tak, asi to opsali)
Celkově se říká, že všechny kondenzované stavy čistých látek (tedy i třeba kapalná rtuť nebo brom pod roztokem) mají jednotkovou aktivitu. 0,01 molární roztok nějaké soli je v podstatě voda o čistotě 99,9%, takže tuto podmínku splňuje.
Osobně se mi to dělení vodou zdá jako dost zesložiťující prvek. Bez něj lze totiž všechny rovnovážné konstanty, ať už acidobazické, součiny rozpustnosti, atp. popsat jednoduchým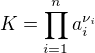 ,
,
kde  je stechiometrický koeficient (z konvence u produktů kladný a u reaktantů záporný).
je stechiometrický koeficient (z konvence u produktů kladný a u reaktantů záporný).
Doučím M, Ch v okolí Pardubic
Press any key to continue. Alt + F4?
Offline

